
| A、d=a+17b | ||
B、C1=
| ||
C、铝为
| ||
| D、与金属反应后剩余盐酸为(C1V1-2b)mol |
| bg |
| 2g/mol |
| C2V2 |
| V1 |
|
|


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、常温常压下,46gN02与N204的混合气体中含有的原子数为3NA | B、15.6 g Na2O2与过量CO2反应时,转移的电子数为O.4NA | C、常温常压下,11.2L 二氧化硫中所含的氧原子数等于NA | D、1L 1 mol?L-1 的Na2CO3溶液中含有NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下,46 g NO2和N2O4的混合气体中含有NA个氮原子 | B、常温常压下,NA个铝原子与足量NaOH溶液反应生成33.6 L H2 | C、1 L 1 mol?L-1的Na2CO3,溶液中含有Na+、CO32-共3NA个 | D、25℃时,1 L pH=1的H2SO4溶液中含有0.2NA个H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 0.1mol?L-1的CuCl2溶液中含Cu2+为0.1NA | B、标准状况下,22.4L CCl4含CCl4分子为NA | C、1mol H3O+含质子数为10NA | D、1mol Na2O和Na2O2混合物中含阴离子的总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.05 | B、0.5 | C、0.55 | D、1.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
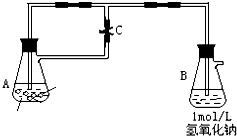 图中为制取纯净且能较长时间存在的Fe(OH)2,药品为铁粉、稀H2SO4,NaOH溶液,当容器A中反应开始后,若分别进行下列操作,请回答有关问题:
图中为制取纯净且能较长时间存在的Fe(OH)2,药品为铁粉、稀H2SO4,NaOH溶液,当容器A中反应开始后,若分别进行下列操作,请回答有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:
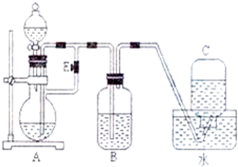 如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及5.00mol?L-1的硫酸,其他试剂任选.填写下列空白:
如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及5.00mol?L-1的硫酸,其他试剂任选.填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂粉精可漂白所有的有色物质 | B、工业上可用植物秸秆生产出乙醇 | C、明矾可以对饮用水进行消毒杀菌 | D、在水中加人催化剂,水变为汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、火力发电站 | B、汽车尾气 | C、大理石场 | D、氯碱工业 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com