
分析 根据CaCO3固体的质量计算其物质的量,再反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O计算相关物理量.
解答 解:10g CaCO3固体的物质的量为$\frac{10g}{100g/mol}$=0.1mol,
(1)由方程式CaCO3+2HCl=CaCl2+CO2↑+H2O可知,0.1mol碳酸钙反应生成0.1mol二氧化碳;
答:生成CO2的物质的量为0.1mol;
(2)由方程式CaCO3+2HCl=CaCl2+CO2↑+H2O可知,0.1mol碳酸钙消耗0.2molHCl,则c=$\frac{n}{V}$=$\frac{0.2mol}{0.2L}$=1mol/L;
答:所用稀盐酸的物质的浓度为1mol/L.
点评 本题考查化学方程式的计算以及物质的量的有关计算,题目难度不大,注意有关计算公式的运用.


科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 研究 目的 | 压强对反应的 影响(P2>P1) | 温度对反应的影响 | 平衡体系增加A 对反应的影响 | 催化剂对反应的影响 |
| 图示 | 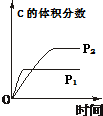 | 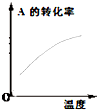 | 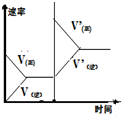 | 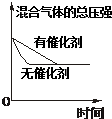 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气可用于自来水杀菌消毒 | B. | 干冰能用于人工降雨 | ||
| C. | 碳酸钙是文物陶瓷的主要成分 | D. | 二氧化硫可用于漂白织物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始时的速率:甲<乙 | |
| B. | 反应所需时间:甲>乙 | |
| C. | 反应开始前,酸的物质的量浓度:甲=乙 | |
| D. | 若使两酸溶液PH都等于5,则加水的体积:甲=乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Fe2十+Cl2═2Fe3++2Cl- | B. | 2Fe2十+O2═2Fe3++2I- | ||
| C. | I2+SO2+2H2O═H2SO4+2HI | D. | SO2+O2+2H2O═H2O2+H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.182 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
| 主要化合价 | +1 | +2 | +2 | +3 | +6、-2 | -1 | -1 |
| A. | D、B简单离子半径大小关系为D3+>B2+ | |
| B. | B2+、D3+、E2-、G-四种离子的核外电子排布相同 | |
| C. | 最高价氧化物对应的水化物的酸性:H2EO4>HFO4 | |
| D. | 气态氢化物的稳定性HG>HF>H2E |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com