
| A、1:1 | B、2:1 |
| C、1:7 | D、2:7 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种气体A与B的摩尔质量比为m:n |
| B、同质量气体A与B气体的分子数比为n:m |
| C、相同状况下,同体积A与B 气体质量比为m:n |
| D、同温、同压下,A气体与B 气体的密度比为n:m |
查看答案和解析>>
科目:高中化学 来源: 题型:
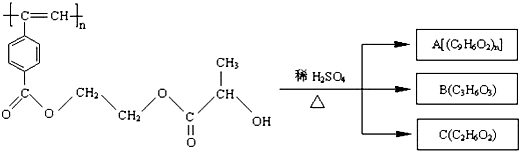
| A、M与A均能使酸性高锰酸钾溶液和溴水褪色 |
| B、B中含有羧基和羟基两种官能团,B能发生消去反应和酯化反应 |
| C、1molM与热的烧碱溶液反应,可消耗2 mol的NaOH |
| D、A、B、C各1mol分别与金属钠反应,放出的气体的物质的量之比为n:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温度同物质的量浓度时,HF比HCN易电离,则等浓度等体积的NaF溶液比NaCN溶液中阴离子总数少 |
| B、0.2 mol?L-l NH4Cl和 0.l mol?L-l NaOH溶液等体积混合后:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) |
| C、0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
| D、相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3?H2O;c(NH4+) 由大到小的顺序是:①>②>④>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
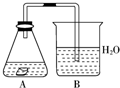 某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如右图所示的装置进行实验,过一段时间后观察.下列现象可能出现的是( )
某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如右图所示的装置进行实验,过一段时间后观察.下列现象可能出现的是( )| A、B中导气管中产生气泡 |
| B、B中导气管里形成一段水柱 |
| C、锥形瓶中溶液无色 |
| D、铁被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在某未知液中加入BaCl2溶液出现白色沉淀,则溶液中肯定有SO42- |
| B、用焰色反应可鉴别出NaCl、KCl和Na2SO4三种物质 |
| C、利用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
| D、在某未知液中加入NaOH溶液后再滴入酚酞试液,若显红色则原溶液中肯定有NH4+离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com