
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验:
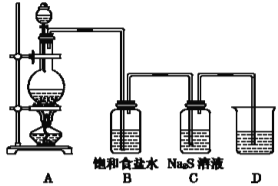
(1)装置A中制取的物质是___,化学方程式___。
(2)装置B的作用是___;C中的现象是___,离子方程式___,由此说明非金属性的强弱顺序是__。
(3)D中盛装的溶液是___,作用是___,离子方程式___。
【答案】Cl2 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 吸收HCl 变浑浊 S2-+Cl2=2Cl-+S↓ Cl>S NaOH溶液 吸收多余的Cl2 Cl2+2OH-=Cl-+ClO-+H2O
MnCl2+Cl2↑+2H2O 吸收HCl 变浑浊 S2-+Cl2=2Cl-+S↓ Cl>S NaOH溶液 吸收多余的Cl2 Cl2+2OH-=Cl-+ClO-+H2O
【解析】
为了验证氯元素的非金属性比硫元素的非金属性强,则装置A应为制取Cl2的装置,其中圆底烧瓶内放置MnO2,分液漏斗内放置浓盐酸;B装置为Cl2中HCl的除杂装置;C中为Cl2与Na2S发生置换反应,从而证明氯的非金属性比硫强的装置;D是尾气的处理装置。
(1)由以上分析可知,装置A中制取的物质是Cl2,发生MnO2与浓盐酸反应,生成MnCl2、Cl2等,化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。答案为:Cl2;MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O。答案为:Cl2;MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)装置B中放置饱和食盐水,是为了除去氯气中的氯化氢,所以其作用是吸收HCl;C中发生硫化钠与氯气的置换反应,生成硫和氯化钠,所以产生的现象是变浑浊(或有淡黄色沉淀生成),离子方程式为S2-+Cl2=2Cl-+S↓,由此说明非金属性的强弱顺序是Cl>S。答案为:吸收HCl;变浑浊;S2-+Cl2=2Cl-+S↓;Cl>S;
(3)D中盛装能吸收氯气的溶液,应是NaOH溶液,作用是吸收多余的Cl2,离子方程式为Cl2+2OH- =Cl-+ClO-+H2O。答案为:NaOH溶液;吸收多余的Cl2;Cl2+2OH-=Cl-+ClO-+H2O。


科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193K,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是
A. S2Cl2的电子式为![]()
B. 固态时S2Cl2属于原子晶体
C. S2Cl2与NaOH的化学方程式可能为:S2Cl2+6NaOH=2NaCl+Na2SO3+Na2S+3H2O
D. S2Cl2是含有极性键和非极性键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于10 mL 0.1 mol·L-1的NH3·H2O溶液,下列说法正确的是( )
A.25 ℃时,若溶液的pH=11,则Kb(NH3·H2O)=1×10-6mol·L-1
B.向溶液中加入少量CH3COONa固体,溶液中的![]() 值变小
值变小
C.向溶液中加入10 mL 0.1 mol·L-1HCl,所得溶液中离子浓度大小顺序为c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.向溶液中加入5 mL 0.1 mol·L-1HCl,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲醇为原料制取高纯H2是重要的研究方向。回答下列问题:
(1)甲醇水蒸气重整制氢主要发生以下两个反应。
主反应:CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g) △H=+49kJ·mol-1
CO2(g)+3H2(g) △H=+49kJ·mol-1
副反应:H2(g)+CO2(g) ![]() CO(g)+H2O(g) △H=+41kJ·mol-1
CO(g)+H2O(g) △H=+41kJ·mol-1
①甲醇在催化剂作用下裂解可得到H2和CO,反应的热化学方程式为__________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是_________________________。
②适当增大水醇比[n(H2O):n(CH3OH)],有利于甲醇水蒸气重整制氢,理由是___________。
③某温度下,将n(H2O):n(CH3OH)=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为_________________(忽略副反应)。
(2)工业上常用CH4与水蒸气在一定条件下来制取H2,其反应原理为:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H=+203kJ·mol-1,在容积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示。
CO(g)+3H2(g) △H=+203kJ·mol-1,在容积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度及压强的关系如图所示。
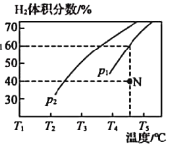
压强为p1时,在N点:v正_______v逆(填“大于”“小于”或“等于”),N点对应温度下该反应的平衡常数K=________mol2·L-2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温、恒容密闭容器中发生反应:Ni(s)+4CO(g)![]() Ni(CO)4(g),△H<0。利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。对该反应的说法正确的是
Ni(CO)4(g),△H<0。利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。对该反应的说法正确的是
A. 增加Ni的量可提高CO的转化率,Ni的转化率降低
B. 缩小容器容积,平衡右移,△H减小
C. 反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低
D. 当4v[Ni(CO)4]=v(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列叙述正确的是( )
A.某氨水的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a<b-1
B.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-)
C.1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0
D.若10mLpH=a的硫酸溶液跟100mLpH=b的NaOH溶液混合后,溶液呈中性,则a+b=13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:NaHSO3溶液呈酸性。常温下,将0.1mol/L亚硫酸(忽略H2SO3的分解)与0.1mol/LNaOH溶液等体积混合,下列关于该混合溶液说法不正确的是( )
A.c(Na+)>c(HSO![]() )>c(H2SO3)>c(SO
)>c(H2SO3)>c(SO![]() )
)
B.c(Na+)=c(HSO![]() )+c(SO
)+c(SO![]() )+c(H2SO3)
)+c(H2SO3)
C.c(HSO![]() )+c(H2SO3)+c(SO
)+c(H2SO3)+c(SO![]() )=0.05mol/L
)=0.05mol/L
D.c(Na+)+c(H+)>c(HSO![]() )+c(SO
)+c(SO![]() )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
A.在0.1molL-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1molL-1Na2CO3溶液中:c(OH-)+c(H+)=c(HCO3-)+2c(H2CO3)
C.向0.2molL-1NaHCO3溶液中加入等体积0.1molL-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1molL-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚醛树脂是1907年世界上第一个合成的高分子材料。它是用酚类(如苯酚)与醛类(如甲醛)在酸或碱的催化下相互缩合而成的。如图是实验室制取酚醛树脂的装置图(该实验所用催化剂为浓盐酸)。下列说法错误的是

A.装置中玻璃导管的作用是冷凝回流
B.试管中发生的反应是:
C.待制备实验结束后,取出试管,冷却至室温,加入适温乙醇,并加热,沉淀溶解,说明酸性条件下制得的酚醛树脂为网状结构
D.实验完毕后,若试管用水不易洗涤,可以加入少量乙醇浸泡几分钟,然后洗净
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com