
| A.开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 |
| B.将煤进行气化处理,提高煤的综合利用效率 |
| C.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 |
| D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
科目:高中化学 来源:不详 题型:单选题
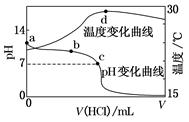
| A.a点由水电离出的c(H+)=1.0×10-14 mol·L-1 |
B.b点:c(NH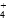 )+c(NH3·H2O)=c(Cl-) )+c(NH3·H2O)=c(Cl-) |
C.c点:c(Cl-)=c(NH ) ) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若pH>7,则一定是c1V1=c2V2 |
| B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C.当pH=7时,若V1=V2,则一定是c2>c1 |
| D.若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H++OH-,在25 ℃时水的离子积为KW=1.0×10-14,在35 ℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )
H++OH-,在25 ℃时水的离子积为KW=1.0×10-14,在35 ℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )| A.c(H+)随着温度的升高而降低 |
| B.35 ℃时c(H+)>c(OH-) |
| C.35 ℃时的水比25 ℃时的水电离程度小 |
| D.水的电离是个吸热过程 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2CO(g) ΔH="-221" kJ·mol-1
2CO(g) ΔH="-221" kJ·mol-1 H2O(l) ΔH="-57.3" kJ·mol-1
H2O(l) ΔH="-57.3" kJ·mol-1| A.C的燃烧热大于110.5 kJ·mol-1 |
| B.①的反应热为221 kJ·mol-1 |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1 |
| D.稀醋酸与稀NaOH溶液反应生成1 mol 水,放出57.3 kJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.c(Na+)>2c(CO32—) |
| B.c(CO32—)>c(OH-)>c(HCO3—)>c(H2CO3) |
| C.c(OH-)=c(H+)+c(HCO3—)+2c(H2CO3) |
| D.c(CO32—)+c(HCO3—)="0.1" mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.H2O(g)=H2(g)+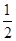 O2(g) ΔH=+242 kJ·mol-1 O2(g) ΔH=+242 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) ΔH=-484 kJ·mol-1 |
C.H2(g)+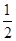 O2(g)=H2O(g) ΔH=+242 kJ·mol-1 O2(g)=H2O(g) ΔH=+242 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g) ΔH=+484 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com