
【题目】某恒温密闭容器发生可逆反应Z(?)+W(?)![]() X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
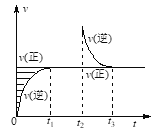
A. Z和W在该条件下至少有一种为气态
B. t1~ t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C. 若在该温度下此反应平衡常数表达式为K=c(X),则t1~ t2时间段与t3时刻后的X浓度不相等
D. 若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而增大
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.增大反应物浓度可增大活化分子百分数,所以反应速率增大
B.放热反应的反应速率一定大于吸热反应的反应速率
C.反应NH3(g) + HCl(g)![]() NH4Cl(s)在室温下可自发进行,则该反应的△H<0
NH4Cl(s)在室温下可自发进行,则该反应的△H<0
D.对于反应X(s)+aY(g)![]() bZ(g)+W(g) △H>0,升高温度,正反应速率增大,逆反应速率减小
bZ(g)+W(g) △H>0,升高温度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. FeCl3+3KSCN![]() Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深
Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深
B. 工业合成氨中,将氨气液化分离
C. A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B中试管中产生气泡快
D. 对于反应2NO2(g)![]() N2O4(g) △H<0,升高温度可使体系颜色变深
N2O4(g) △H<0,升高温度可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将下列硅酸盐改写成氧化物的形式(改写时注意金属氧化物在前,非金属氧化物在后,低价在前,高价在后)。
①镁橄榄石(Mg2SiO4)____________。
②高岭石Al2(Si2O5)(OH)4____________。
(2)除去铜表面的铜绿[Cu(OH)2CO3]选用试剂____________,反应方程式为____________。
(3)在![]() 中:____________和____________互为同位素;_____和________中子数相等,共有________种原子,属于________种元素。
中:____________和____________互为同位素;_____和________中子数相等,共有________种原子,属于________种元素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1mol/L的某一元酸HR溶液中逐滴加入0.1mol/L氨水,所得溶液pH及导电能力变化如图。下列分析不正确的是( )

A. a~b点导电能力增强说明HR为弱酸
B. a、b点所示溶液中水的电离程度不相同
C. b恰好完全中和,pH=7说明NH4R没有水解
D. c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氢气通入10 g 氧化铜粉末加热片刻,冷却后剩余固体的质量为8.4 g,下列计算正确的是
A. 有1.6 g 水生成
B. 有8.4 g 铜生成
C. 有80%的氧化铜被还原
D. 实验时所消耗的氢气不足0.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)(已知:2SO2+O2![]() 2SO3),反应过程中的能量关系可用如图简单表示(图中的△H 表示生成1mol产物的数据). 下列说法正确的是( )
2SO3),反应过程中的能量关系可用如图简单表示(图中的△H 表示生成1mol产物的数据). 下列说法正确的是( )

A. S8的燃烧热△H=﹣a kJ·mol﹣1
B. 1 mol SO2和过量 O2反应可释放出 b kJ 的热量
C. 已知1个S8分子中有8个S﹣S,S=O的键能为d kJ·mol﹣1,O=O的键能为e kJ·mol﹣1,则S8分子中S﹣S的键能为(2d﹣a﹣e) kJ·mol﹣1
D. 若使用V2O5作催化剂,当SO2(g)转化生成1mol SO3(g)时,释放的热量小于b kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(Te)的单质和化合物在化工生产等方面具有重要应用。
(1)下列关于碲及其化合物的叙述不正确的是_______。
A.Te位于元素周期表的第五周期ⅣA族
B. Te的氧化物通常有TeO2和TeO3
C. H2TeO4的酸性比H2SO4酸性强
D.热稳定性H2Te比H2S弱,H2Te比HI强
(2)25℃时,亚碲酸(H2TeO3)的 ![]() = 1×10-3,
= 1×10-3, ![]() =2×10-8。0. 1 mol . L-1H2TeO3 的电离度 a 约为___________ (
=2×10-8。0. 1 mol . L-1H2TeO3 的电离度 a 约为___________ (![]() ); NaHTeO3的溶液的pH_______7(填“>”、“=”或“<”)。
); NaHTeO3的溶液的pH_______7(填“>”、“=”或“<”)。
(3)TeO2微溶于水,易溶于较浓的强酸和强碱。工业上常用铜阳极泥(主要含有TeO2、少量Ag、Au)为原料制备单质碲,其工艺流程如下:

①“碱浸”时TeO2发生反应的化学方程式为 _________。
②“沉碲”时控制溶液的pH为4. 5~5. 0,生成Tea沉淀。酸性不能过强的原因是_________;防止局部酸度过大的操作方法是____________。
③“酸溶”后,将SO2通入TeCl4酸性溶液中进行“还原”得到碲,该反应的化学方程式是____________。
④工业上还可以通过电解铜阳极泥碱浸、过滤后的滤液得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述中正确的是( )

A.图Ⅰ所示电池中,负极电极反应为Zn-2e-![]() Zn2+
Zn2+
B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中被还原为Ag
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com