
在一定温度下、一定体积条件下,能说明下列反应达到平衡状态的是( )
A.反应2SO2(g)+O2(g)
 2SO3(g) 容器内的密度不随时间变化
2SO3(g) 容器内的密度不随时间变化
B.反应A2(g)+B2(g)
 2AB(g)容器内的总压强不随时间变化
2AB(g)容器内的总压强不随时间变化
C.反应N2+3H2 2NH3容器内气体平均相对分子质量不随时间变化
2NH3容器内气体平均相对分子质量不随时间变化
D.反应4A(s)+3B(g)
 2C(g)+D(g)容器内气体平均相对分子质量不随时间变化
2C(g)+D(g)容器内气体平均相对分子质量不随时间变化
CD
【解析】
试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。密度是混合气的质量和容器容积的比值,A中在反应过程中质量和容积始终是不变的,不能说明;B中反应前后气体体积是不变的,所以压强也是始终不变的,B不正确;混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,C中质量不变,但物质的量是变化的,而D中物质的量不变,但气体的质量是变化的,所以都可以说明,答案选CD。
考点:考查化学平衡状态的判断
点评:判断化学平衡状态的标志有:(1)任何情况下均可作为标志的:①υ正=υ逆(同一种物质);②各组分含量(百分含量、物质的量、质量)不随时间变化;③某反应物的消耗(生成)速率、某生成物的消耗(生成)速率=化学计量数之比;(2)在一定条件下可作为标志的是:①对于有色物质参加或生成的可逆反应体系,颜色不再变化;②对于有气态物质参加或生成的可逆反应体系,若反应前后气体的系数和相等,则混合气体平均相对分子质量M和反应总压P不变(恒温恒容);③对于恒温绝热体系,体系的温度不在变化;(3)不能作为判断标志的是:①各物质的物质的量或浓度变化或反应速率之比=化学计量数之比 (任何情况下均适用);②有气态物质参加或生成的反应,若反应前后气体的系数和相等,则混合气体平均相对分子质量M和反应总压P不变(恒温恒容)。


科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物 A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多。该化合物具有如下性质:
① 在25℃时,电离常数K1=3.99×10-4,K2=5.5×10-6
②A+RCOOH(或ROH)![]() 有香味的产物
有香味的产物
③1molA![]() 慢慢产生l.5mol气体
慢慢产生l.5mol气体
④A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:(l)根据以上信息,对A的结构可作出的判断是 (多选扣分)
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)有机物A的结构简式(不含-CH3)为
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:
(4)A的一个同类别的同分异构体是
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省四校高二(上)期末化学试卷(仙桃中学、麻城一中、新洲一中、武汉二中)(解析版) 题型:解答题
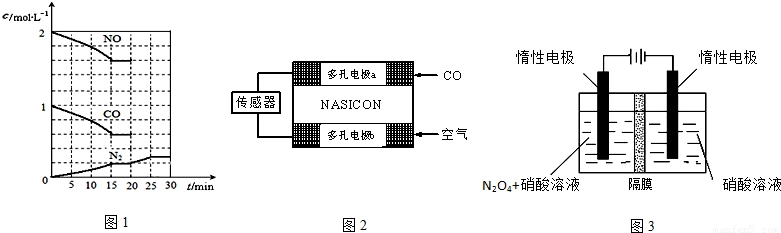
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省黄冈市高一(下)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物 A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多。该化合物具有如下性质:
① 在25℃时,电离常数K1=3.99×10-4,K2=5.5×10-6
②A+RCOOH(或ROH)![]() 有香味的产物
有香味的产物
③1molA![]() 慢慢产生l.5mol气体
慢慢产生l.5mol气体
④A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:(l)根据以上信息,对A的结构可作出的判断是 (多选扣分)
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)有机物A的结构简式(不含-CH3)为
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:
(4)A的一个同类别的同分异构体是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com