
 Fe��OH��3�����壩+3H+�����ɵ�����Fe��OH��3�����������ˮ�е��������ʣ��ﵽ��ˮ��Ŀ�ģ�
Fe��OH��3�����壩+3H+�����ɵ�����Fe��OH��3�����������ˮ�е��������ʣ��ﵽ��ˮ��Ŀ�ģ����� ������ˮ�����ɽ��壬�ɾ���ˮ��������Һ�����������ӵ�ˮ�⣬���������������������ظ�������ӷ���������ԭ��Ӧ���Դ������
��� �⣺Fe2��SO4��3 ��ˮ��ԭ����Fe3++3H2O  Fe��OH��3�����壩+3H+�����ɵ�����Fe��OH��3�����������ˮ�е��������ʣ��ﵽ��ˮ��Ŀ�ģ�
Fe��OH��3�����壩+3H+�����ɵ�����Fe��OH��3�����������ˮ�е��������ʣ��ﵽ��ˮ��Ŀ�ģ�
ʹ��ʱ����Fe2��SO4��3 ������ʹ���Է�ˮ�е������������ȥ����ԭ������Ϊ�����Է�Һ�У�H+������Fe3+��ˮ�⣬���õ�Fe��OH��3���壬���Բ��ܹ����������
�����Ի����£����ظ�����ķ�ˮ�м���FeSO4��Һ��Ȼ�����pH��ʹ���ɵ�Cr3+ת��ΪCr��OH��3����һ����Ӧ�����ӷ���ʽΪCr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O��
�ʴ�Ϊ��Fe3++3H2O  Fe��OH��3�����壩+3H+�����ɵ�����Fe��OH��3�����������ˮ�е��������ʣ��ﵽ��ˮ��Ŀ�ģ���Ϊ�����Է�Һ�У�H+������Fe3+��ˮ�⣬���õ�Fe��OH��3���壬���Բ��ܹ����������Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O��
Fe��OH��3�����壩+3H+�����ɵ�����Fe��OH��3�����������ˮ�е��������ʣ��ﵽ��ˮ��Ŀ�ģ���Ϊ�����Է�Һ�У�H+������Fe3+��ˮ�⣬���õ�Fe��OH��3���壬���Բ��ܹ����������Cr2O72-+6Fe2++14H+�T2Cr3++6Fe3++7H2O��
���� ���⿼������ˮ�⼰������ԭ��Ӧ��Ϊ��Ƶ���㣬����ˮ�ⷴӦ��Ӧ�á�������ԭ��Ӧ��Ӧ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�ⷴӦԭ����Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
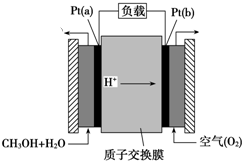
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 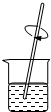 ���� | B�� | 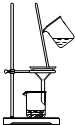 �ܽ� | C�� | 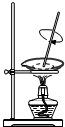 ���� | D�� |  ��ɫ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.012 kg 12C�к���Լ 6.02��1023 ��̼ԭ�� | |
| B�� | 1 mol H2O���2 mol���1 mol�� | |
| C�� | �������Ƶ�Ħ����������������Է������� | |
| D�� | 2 molˮ��Ħ��������1 molˮ��Ħ��������2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
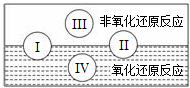 ������ԭ��Ӧ�������������о��й㷺����;���ᴩ�Ž�
������ԭ��Ӧ�������������о��й㷺����;���ᴩ�Ž�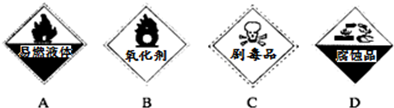
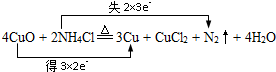 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �������ʽ��CH | B�� | ������ӵı���ģ�ͣ�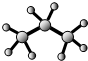 | ||
| C�� | ��ϩ�Ľṹ��ʽ��CH2CH2 | D�� | ��ȩ�Ľṹʽ��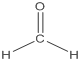 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ԭ�� | B�� | Ԫ�������� | C�� | ʯ�͵ijɷ� | D�� | ����ƽ�ⳣ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
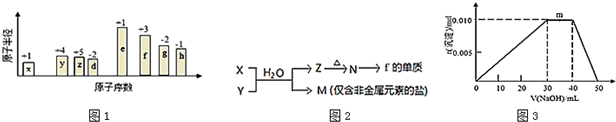
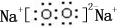 ��B�dz�����Һ̬�������ϡ��Һ�ױ����ֽ⣬��ʹ�õĴ���ΪAB��������ţ�
��B�dz�����Һ̬�������ϡ��Һ�ױ����ֽ⣬��ʹ�õĴ���ΪAB��������ţ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com