
NH4Al(SO4)2·12H2O的相对分子质量为453。欲配制100 mL pH为2、浓度约为0.1 mol·L-1的NH4Al(SO4)2溶液,配制过程为
①用托盘天平称量NH4Al(SO4)2·12H2O固体 g;
②将上述固体置于烧杯中, 。
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
结晶玫瑰是具有强烈玫瑰香气的香料,可由下列反应路线合成(部分反应条件略去):
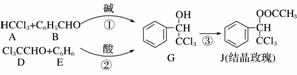
(1)A的类别是________,能与Cl2反应生成A的烷烃是________。B中的官能团是________。
(2)反应③的化学方程式为__________________________________________________。
(3)已知:B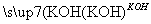 苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液,能除去的副产物是________________。
苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液,能除去的副产物是________________。
(4)已知: 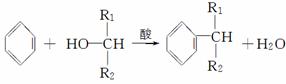 则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为________。
则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和应用正确的是( )
A.油脂在酸性条件下水解生成高级脂肪酸和甘油
B.福尔马林可防腐,可用它保存海鲜产品
C.乙醇、糖类和蛋白质都是人体必需的营养物质
D.合成橡胶与光导纤维都属于有机高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
用溶质质量分数为98%的浓硫酸和溶质质量分数为18%的稀硫酸配制500 g溶质质量分数为28%的硫酸,需要浓硫酸和稀硫酸的质量分别为( )
A.62.5 g 437.5 g B.71.4 g 428.6 g
C.437.5 g 62.5 g D.428.6 g 71.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
请填写下列物质的结晶方法。
(1)氯化钠: 。
(2)硝酸钾: 。
(3)硫酸铜晶体: 。
(4)从FeCl3溶液中得到FeCl3·6H2O固体 。
查看答案和解析>>
科目:高中化学 来源: 题型:
20 ℃时,饱和NaCl溶液的密度为ρ g·cm-3,物质的量浓度为c mol·L-1,则下列说法中错误的是( )
A.温度低于20 ℃时,饱和NaCl溶液的浓度小于c mol·L-1
B.20 ℃时,饱和NaCl溶液的质量分数为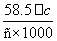 ×100%
×100%
C.20 ℃时,密度小于ρ g·cm-3的NaCl溶液是不饱和溶液
D.20 ℃时,饱和NaCl溶液的溶解度S=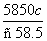 g/100 g水
g/100 g水
查看答案和解析>>
科目:高中化学 来源: 题型:
奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是食品与硫酸和催化剂一同加热,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
①样品处理:准确称取一定量的固体样品奶粉,移入干燥的烧杯中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
②NH3的蒸馏和吸收:把制得的溶液(取一定量)通过定氮装置,经过一系列的反应,使氨变成硫酸铵,再经过碱化蒸馏后,氨即成为游离态,游离氨经硼酸吸收。
③氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,由消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大 (填字母)。
A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯
B.定容时,俯视刻度线
C.定容时,仰视刻度线
D.移液时,有少量液体溅出
(2)若称取样品的质量为1.5 g,共配制100 mL的溶液,取其中的20 mL,经过一系列处理后,使N转变为硼酸铵后用0.1 mol·L-1盐酸滴定,其用去盐酸的体积为23.0 mL,则该样品中N的含量为 (保留两位小数)。
[已知:滴定过程中涉及到的反应方程式:(NH4)2B4O7+2HCl+5H2O===2NH4Cl+4H3BO3]
查看答案和解析>>
科目:高中化学 来源: 题型:
氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子构型为平面三角形,则其阳离子的构型和阳离子中氮的杂化方式为( )
A.直线 sp杂化 B.V型 sp2杂化
C.三角锥形 sp3杂化 D.平面三角形 sp2 杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com