
分析 (1)①根据△G=△H-T△S判断,△G<0,反应自发进行.
②反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度、含量等不再发生变化,以及由此衍生的其它量不变,可由此进行判断.
(2)依据反应是吸热反应,升温平衡向吸热反应方向进行分析;
(3)若不改变H2、CO的量,由图可知,t4时瞬间正、逆反应都增大,平衡向逆反应移动,改变条件为压缩体积增大压强;t6时瞬间正、逆反应都增大,平衡不移动,故应是加入催化剂,t2时改变改变条件,平衡向正反应移动,在t3时重新到达平衡,t4时改变条件,平衡向逆反应移动,t5时由达平衡,故t3~t4平衡状态CO的含量最高;
解答 解:(1)①由热化学反应方程式可知,反应为焓增,熵增过程,即△H>0、△S>0,△G=△H-T△S<0反应自发进行,所以该反应自发进行,受温度影响,298℃时,△H=+131.3kJ•mol-1△S=+133.7J•mol-1•K-1,△G=△H-T△S=+131.3kJ•mol-1-(298+273)K×(+133.7×10-3KJ•mol-1)•K-1=54.96KJ/mol>0,说明反应非自发进行;
故答案为:不能;
②C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,反应是气体体积增大的吸热反应,
a.一定温度下,在一个容积可变的密闭容器中发生上述反应,反应前后气体的物质的量发生变化,随反应进行气体的物质的量增加,压强增大,保持恒压,容器中的压强始终不变,不能说明反应到达平衡,故a错误;
b.1 molH-H键断裂的同时断裂2mol H-O键,断裂2mol H-O键同时生成l molH-H键,说明反应到达平衡,故b正确.
c.反应速率之比等于化学方程式计量数之比,v正(CO)=v逆(H2O),说明水的正反应速率和逆反应速率相同,反应达到平衡状态,故c正确;
d.根据反应可知,自始至终c(CO)=c(H2),不能说明反应到达平衡,故d错误;
e.反应前后气体的物质的量发生变化,容器内气体总物质的量不变,说明反应达到平衡状态,故e正确;
故选:bce.
(2)反应是吸热反应,升温平衡正向进行,平衡常数增大;
故答案为:增大;
(3)若不改变H2、CO的量,由图可知,t4时瞬间正、逆反应都增大,平衡向逆反应移动,改变条件为压缩体积增大压强;t6时瞬间正、逆反应都增大,平衡不移动,故应是加入催化剂,t2时改变改变条件,平衡向正反应移动,在t3时重新到达平衡,t4时改变条件,平衡向逆反应移动,t5时由达平衡,故t3~t4平衡状态CO的含量最高;
故答案为:增大压强,t3~t4;
点评 本题考查化学平衡常数与影响因素、平衡状态判断、影响平衡移动的因素与平衡图象等,比较基础,注意方程式中物质的状态,理解外界条件对反应速率的影响,题目难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
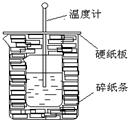 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH-12e-+12OH-═2CO2+9H2O | B. | O2+4H++4e-═2H2O | ||
| C. | O2+2H2O+4e-═4OH- | D. | C2H5OH+16OH--12e-═2CO32-+11H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Si可用于制造太阳能电池 | |
| B. | Na2O2可用于呼吸面具中作为氧气的来源 | |
| C. | Fe2O3常用于制造红色油漆和涂料 | |
| D. | 常温下可用铝制容器盛装稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 对于mA(s)+nB(g)?pC(g)+Q的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )
对于mA(s)+nB(g)?pC(g)+Q的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )| A. | m+n<p | B. | n>p | ||
| C. | x点的状态是v正>v逆 | D. | 以上答案都错误 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含1molFeCl3 的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 12克金属镁与足量的盐酸反应,转移电子数一定为NA(已知:Mg-2e-═Mg2+) | |
| C. | 10.6克Na2CO3晶体中含Na+数目为0.2NA | |
| D. | 常温常压下,22克CO2和0.5NA个CH4分子的体积是相等的 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 现象 | 结论 | 离子方程式 |
| 第一步 | 取2-3mL溶液装于试管,向试管中加入几滴KSCN溶液. | 若溶液变红色,则溶液含有Fe3+; 若无现象,则不含Fe3+ | Fe3++3SCN-=Fe(SCN)3 |
| 第二步 | 另取少量溶液装于试管,向试管里滴加几滴酸性高锰酸钾溶液 | 若溶液紫色褪去,则溶液含有Fe2+; 若无明显变化,则不含Fe3+. | 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 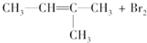 → → | |
| B. | CH2═CH-CH2-CH3+HCl$→_{△}^{催化剂}$ | |
| C. | CH3-CH═CH2+H2O$→_{加热、加压}^{催化剂}$ | |
| D. | nCH2═CH2+nCH2═CH-CH3$→_{△}^{催化剂}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com