
【化学一一选修5:有机化学基础】(15分)
某药物可通过以下方法合成:
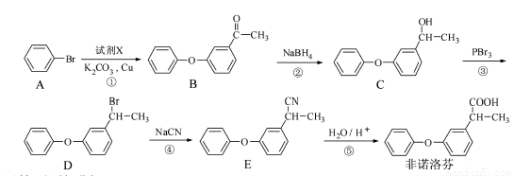
注:非诺洛芬是一种治疗类风湿性关节炎的药物。请回答下列问题:
(1)非诺洛芬中的含氧官能团为 和 (填名称)。
(2)反应①中加入的试剂X的分子式为C8H8O2,X的结构简式为 。
(3)在上述五步反应中,属于取代反应的是 (填序号)。
(4)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环。
写出该同分异构体的结构简式: 。
(5)根据已有知识并结合相关信息,写出以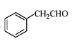 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源:2016届江西省红色七校高三上学期第一次联考化学试卷(解析版) 题型:选择题
可逆反应aA(g)+bB(s) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是

A.升高温度,平衡向逆反应方向移动
B.使用催化剂,C的物质的量分数增加
C.化学方程式系数a>c+d
D.根据图像无法确定改变温度后平衡移动方向
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期9月月考化学试卷(解析版) 题型:选择题
有关化学用语正确的是
A.质子数27的钴-60原子: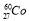
B.氯化铵的电子式:
C.S2-的结构示意图:
D.Cl-的电子排布式:1s22s22p63s23p5
查看答案和解析>>
科目:高中化学 来源:2016届湖南省常德市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列各组离子在指定的溶液中能大量共存的是
①无色溶液中:K+、Cu2+、Na+、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
③加入Al能放出H2的溶液中:Cl-、HCO3-、NO3-、NH4+
④在由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、I-
⑤能使红色石蕊试纸变为蓝色的溶液:Na+、Cl-、S2-、ClO-
⑥酸性溶液中:Fe2+、Al3+、NO3-、Cl-
A.①②⑤ B.③⑤⑥ C.②④ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2016届湖南省长沙市高三上学期第三次月考化学试卷(解析版) 题型:实验题
(12分)老师用下图所示装置为同学们做了一个兴趣实验。已知装置B、C、D中依次盛有紫色石蕊试液、足量的澄清石灰水和稀盐酸。小资料:HCl气体极易溶于水。

(1)打开A中的玻璃塞和活塞,B中实验现象是 。B中的现象不能说明二氧化碳与水反应的原因是 。C中的化学反应的方程式是 。
(2)一段时间后,关闭A中的活塞和玻璃塞,打开弹簧夹K2及E中的玻璃塞和活塞,待足量的过氧化氢溶液流入锥形瓶后,立即关闭E中的活塞,并用弹簧夹K2夹紧橡皮管。C中可能出现的现象是 ,解释C中呈现的现象的原因是 。
(3)将A中产生的气体通入过量的NaOH溶液中,为了确定反应后的溶液中含有NaOH 的实验方法为 。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省兴义市高三上学期期中测试理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是:
A.过量氯气通入溴化亚铁溶液中:Fe2++2Br-+2Cl2=Fe3++Br2+4Cl-
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
C.碳酸氢钙和过量的氢氧化钠溶液反应:Ca2++ OH—+HCO3—=CaCO3↓+ H2O
D.用FeCl3溶液腐蚀印刷电路板:Cu+Fe3+=Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期第一次月考化学试卷(解析版) 题型:填空题
(每空2分,共10分)实验室里要配制400mL0.2mol/L的硫酸钠溶液。实验步骤大致有:
A.在天平上称出___________g硫酸钠固体,把它放在烧杯里,用适量的蒸馏水溶解。
B.把得到的溶液小心地沿着玻璃棒注入________mL的容量瓶中。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也小心转入容量瓶中。
D.继续向容量瓶中加蒸馏水至液面距刻度l~2cm处,改用_______________小心滴加蒸馏水至溶液凹液面底部与刻度线水平相切。
E.将瓶塞塞紧,充分摇匀。
F.将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶。
(1)请填写上述空白处。
(2)下列情况会使所配溶液浓度偏高的是___________(填序号)。
①容量瓶用前内壁沾有水珠 ②没有进行上述的操作步骤C ③未冷却到室温就注入容量瓶定容 ④定容时,水加多了,用滴管吸出 ⑤定容时,仰视容量瓶刻度线 ⑥定容时,俯视容量瓶刻度线
(3)如果实验室用98%的浓硫酸(密度为1.8g·cm-3) 配制 3.6mol·L-1的稀硫酸150mL。计算所需浓硫酸的体积为___________mL。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期第二次月考化学试卷(解析版) 题型:填空题
某消毒液的主要成分为 NaClO(混有少量NaCl),请用相应的化学用语来解释下列事实。
(1)该消毒液可用NaOH 溶液吸收Cl2 制备,化学方程式为_______________________。
(2)该消毒液的pH 约为12,离子方程式为__________________________。
(3)向FeSO4 溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为______________。
(4)该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。每产生1 mol Cl2(标准状况下),转移电子个数约为________________ 。
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
碘是一种与人的生命活动密切相关的元素,已知I2能溶于NaOH或KI溶液,反应方程式分别为:3I2+6OH﹣═5I﹣+IO3-+3H2O(HIO不稳定,易发生歧化反应)和I2+I﹣═I3-,溴化碘(IBr)是一种卤素互化物,具有与卤素单质相似的性质,下列反应方程式中不正确的是
A.IBr加入Na2S溶液中产生黄色浑浊:IBr+S2﹣═I﹣+Br﹣+S↓
B.IBr加入KI溶液中:IBr+2I﹣═Br﹣+ I3-
C.IBr加入NaOH溶液中:IBr+2OH﹣═BrO﹣+I﹣+H2O
D.IBr加入AgNO3溶液中:3IBr+5Ag++3H2O═3AgBr↓+2AgI↓+ IO3-+6H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com