
| A. | 反应KIO3+6HI=KI+3H2O+3I2,生成3mol I2转移电子的总数为6NA | |
| B. | 标准状况下,由0.4 mol H2O2生成O2转移的电子数目为0.2NA | |
| C. | 12g石墨和C60的混合物中质子总数为6NA | |
| D. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
分析 A.氧化还原反应中,同种元素化合价向中间靠拢,则碘酸钾中碘元素被还原成碘单质,据此进行计算;
B.双氧水中氧元素化合价为-1价,0.4mol双氧水完全分解生成0.2mol氧气,转移了0.4mol电子;
C.石墨和C60的混合物都是有C原子构成,计算出12gC的物质的量,再计算出含有的质子总数;
D.氢氧化钠溶液中,氢氧根离子抑制了水的电离,溶液中的氢离子是水电离的.
解答 解:A.反应KIO3+6HI=KI+3H2O+3I2中,KIO3的+5价碘元素被还原成0价的碘单质,则生成3mol I2转移了5mol电子,转移电子的总数为5NA,故A错误;
B.0.4mol双氧水完全分解生成0.2mol氧气,双氧水中氧元素的化合价为-1价,则生成0.2mol氧气转移了0.4mol电子,转移的电子数为0.4NA,故B错误;
C.12g石墨和C60的混合物中含有12gC,含有1molC原子,则混合物中含有6mol质子,含有的质子总数为6NA,故C正确;
D.室温下,1L pH=13的NaOH溶液中,氢氧根离子浓度为0.1mol/L,氢氧化钠溶液中的氢离子是水电离的,则水电离的氢氧根离子浓度为1×10-13mol/L,1L该溶液中含有水电离的氢氧根离子的物质的量为1×10-13mol,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度中等,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的转化关系为解答关键,A为易错点,注意正确分析该反应中元素化合价变化情况.


科目:高中化学 来源: 题型:选择题
| A. | NH4+,Ag+,NO3-,CO32-,SO42- | B. | Fe2+,H+,NO3-,Cl- | ||
| C. | Al3+、NH4+,HCO3-、Cl- | D. | K+、Na+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
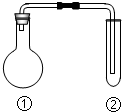 下列选项中的反应、现象与结论完全一致的是(夹持、加热装置已略去)( )
下列选项中的反应、现象与结论完全一致的是(夹持、加热装置已略去)( )| ①中的反应 | ②中的现象 | 结论 | |
| A | MnO2与浓盐酸加热 | KI淀粉溶液很快变蓝 | Cl2有氧化性 |
| B | Cu与浓硫酸加热 | 溴水褪色 | SO2有漂白性 |
| C | Na2CO3与醋酸溶液 | 苯酚钠溶液变浑浊 | 酸性:碳酸>苯酚 |
| D | 电石与饱和食盐水 | 酸性高锰酸钾溶液褪色 | 乙炔有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 测0.01mol/L的醋酸的pH为5:CH3COOH?CH3COO-+H+ | |
| B. | 电解饱和食盐水,产生气体:2Cl-+2H2O$\frac{\underline{\;高温\;}}{\;}$Cl2↑+2OH-+H2↑ | |
| C. | 铁放在氧气中燃烧,产生黑色固体:4Fe+3O 2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| D. | 硫酸钙与碳酸钠溶液,产生白色沉淀:CaSO4(S)+CO32-?CaCO3(S)+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z | R | |
| 主要化合价 | -4,+4 | -4,+4 | -2,+6 | -1,+7 |
| A. | 非金属性:Z<R<Y | |
| B. | T与R可以形成化合物:TR2 | |
| C. | X与R的单质均能使品红溶液褪色,且褪色原理相同 | |
| D. | T的最高价氧化物的水化物分别能与X、Y、Z的最高价氧化物反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量SO2:Na+、S2-、OH-、AlO2- | B. | 通入足量CO2:K+、Ca2+、Cl-、NO3- | ||
| C. | 通入足量Cl2:SO2、Ba2+、Cl-、K+ | D. | 通入足量NH3:Fe3+、Cl-、Ba2+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 元素X有三种同位素 | |
| B. | 其中一种同位素质量数为36 | |
| C. | 质量数为35的同位素原子的质量分数为75% | |
| D. | 元素单质X2的平均式量为71 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com