
| A、溴水溶液Na+ K+ NO3- CH3CHO |
| B、氢氧化钠溶液AlO2- K+ Cl- NO3- |
| C、氢氧化铁胶体H+ K+ S2- Cl- |
| D、高锰酸钾溶液H+ Na+ SO42- CH3CH2OH |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液的体积(mL) | 标准溶液的体积 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.01 | 22.00 |
| 3 | 25.00 | 0.22 | 20.22 |
查看答案和解析>>
科目:高中化学 来源: 题型:
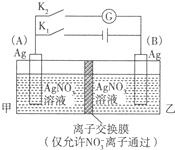 利用如图装置进行实验,甲乙两池均为1mol?L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K1,断开K2.一段时间后,断开K1,闭合K2,形成浓差电池,电流计指针偏转(Ag+浓度越大氧化性越强).下列说法不正确的是( )
利用如图装置进行实验,甲乙两池均为1mol?L-1的AgNO3溶液,A、B均为Ag电极.实验开始先闭合K1,断开K2.一段时间后,断开K1,闭合K2,形成浓差电池,电流计指针偏转(Ag+浓度越大氧化性越强).下列说法不正确的是( )| A、闭合K1,断开K2后,A电极增重 |
| B、闭合K1,断开K2后,乙池溶液浓度上升 |
| C、断开K1,闭合K2后,NO3-向B电极移动 |
| D、断开K1,闭合K2后,A电极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、将溶液稀释,
| ||
| B、滴入含0.1 mol CH3COOH的溶液:c(CH3COO-)<c(HCO3-) | ||
| C、通入0.1 mol CO2气体,溶液中存在:c(Na+)=c(CO32-)十c(HCO3-)+c(H2CO3) | ||
| D、滴入酚酞,微热,溶液颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、以Y浓度变化表示的反应速率为0.0005mol/(L?s) | ||
B、其他条件不变,将容器体积扩大至20L,则Z的平衡浓度变为原来的
| ||
| C、其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大 | ||
| D、其他条件不变,升高温度逆反应速率加快,正反应速率减慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H+ | ||
|
| Fe2+ | ||
|
| OH- | ||
|
| A、在第①反应平衡体系中加入水,溶液中c(H+)增大 |
| B、溶液的pH值不变时,说明第①步反应达平衡状态 |
| C、第②步中,还原0.01mol Cr2O72-离子,需要0.06mol的FeSO4?7H2O |
| D、上述三步转化反应中,只有一个反应为氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、雾霾天气中的主要污染物是PM2.5,其中含氮的有机物和光发生化学作用,可形成光化学烟雾 |
| B、砷是水污染的重要因素之一,其最高价含氧酸砷酸的酸性比磷酸酸性弱 |
| C、土壤污染物可分为无机污染物和有机污染物,农药污染多为有机污染物 |
D、苏丹红是人工合成的一种工业染料,若掺入饲料中饲养禽类会污染蛋类食品,它的结构简式是 ,其分子式是:C22H18N4O ,其分子式是:C22H18N4O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 生产生活中广泛涉及氧化还原反应.
生产生活中广泛涉及氧化还原反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com