
【题目】2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰,表彰他们对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
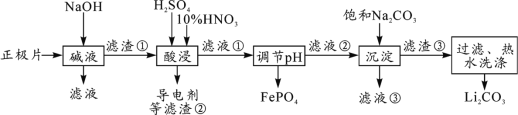
(1)从“正极”可以回收的金属有___________________。
(2)“碱溶”时Al箔溶解的离子方程式_________________________。
(3)“酸浸”时产生标准状况下2.24L NO时,则被氧化的LiFePO4为_________mol。(其他杂质不与HNO3反应)
(4)实验测得滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,Li+的沉降率到99%,则滤液③中c(CO![]() )=________mol·L-1。 [Ksp(Li2CO3)=1.6×10-3]
)=________mol·L-1。 [Ksp(Li2CO3)=1.6×10-3]
(5)磷酸亚铁锂电池总反应为:LiFePO4+6C ![]() Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。放电时,正极反应式为________________________。
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。放电时,正极反应式为________________________。
(6)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取1.40g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030 mol·L-1重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00mL。
已知:2Fe3++Sn2++6Cl-= SnCl![]() +2Fe2+
+2Fe2+
4Cl-+Sn2++2HgCl2= SnCl![]() +Hg2Cl2
+Hg2Cl2
6Fe2++Cr2O![]() +14H+ = 6Fe3++2Cr3++7H2O
+14H+ = 6Fe3++2Cr3++7H2O
①实验中加入HgCl2饱和溶液的目的是________________________。
②磷酸亚铁锂电池中铁的含量为_______________。
【答案】Li、Fe、Al ![]() 0.3mol 4
0.3mol 4 ![]() 将溶液中过量的Sn2+转化为稳定的络合物SnCl
将溶液中过量的Sn2+转化为稳定的络合物SnCl![]() ,防止Fe2+的干扰 28.8%
,防止Fe2+的干扰 28.8%
【解析】
(1)根据元素守恒,即根据正极片中含有金属元素,其余导电剂中所含元素不明,均能通过一定方法进行回收再利用。
(2)“碱溶”时是Al箔与NaOH溶液反应,该离子方程式要求识记。
(3)“酸浸”时是硝酸将LiFePO4被氧化为FePO4,根据得失电子总数相等,即可进行求解。
(4)本题根据难溶电解质的溶度积进行计算即可,特别提醒是溶液中c(Li+)从4 mol·L-1因加入了等体积的Na2CO3溶液后变为2mol·L-1。
(5)放电时正极发生还原反应,结合题干中总反应分析不难得出正极反应式。
(6)根据题干的三个反应式可以得出Sn2+的还原性比Fe2+的强,HgCl2饱和溶液将Sn2+转化为更稳定的络离子SnCl![]() , 由反应6Fe2++Cr2O
, 由反应6Fe2++Cr2O![]() +14H+ = 6Fe3++2Cr3++7H2O即可进行铁元素质量分数的求算。
+14H+ = 6Fe3++2Cr3++7H2O即可进行铁元素质量分数的求算。
(1)根据元素守恒,正极片中含有Li、Fe、Al三种金属元素,均能通过一定方法进行回收再利用,故答案为:Li、Fe、Al;
(2)“碱溶”时Al箔与NaOH溶液反应的离子方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)“酸浸”时是硝酸被还原产生NO,LiFePO4被氧化为FePO4,根据得失电子总数相等可知:![]() ,故答案为:0.3mol;
,故答案为:0.3mol;
(4)实验测得滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,则溶液中的c(Li+)=2mol·L-1,Li+的沉降率到99%,溶液中剩余的c(Li+)=2mol·L-1![]() 1%=0.02mol/L,则滤液③中
1%=0.02mol/L,则滤液③中 ,故答案为:4.0;
,故答案为:4.0;
(5)放电时正极发生还原反应,分析总反应:LiFePO4+6C ![]() Li1-xFePO4+LixC6,可以得出正极反应式为
Li1-xFePO4+LixC6,可以得出正极反应式为![]() ,故答案为:
,故答案为:![]() ;
;
(6)①有反应:2Fe3++Sn2++6Cl-= SnCl![]() +2Fe2+,可知Sn2+的还原性比Fe2+的强,当有Sn2+存在时,Cr2O
+2Fe2+,可知Sn2+的还原性比Fe2+的强,当有Sn2+存在时,Cr2O![]() 首先氧化Sn2+,故必须将Sn2+转化为更稳定的络离子SnCl
首先氧化Sn2+,故必须将Sn2+转化为更稳定的络离子SnCl![]() ,否则影响Fe2+的测量,故实验中加入HgCl2饱和溶液的目的是将溶液中过量的Sn2+转化为稳定的络合物SnCl
,否则影响Fe2+的测量,故实验中加入HgCl2饱和溶液的目的是将溶液中过量的Sn2+转化为稳定的络合物SnCl![]() ,防止Fe2+的干扰,故答案为:将溶液中过量的Sn2+转化为稳定的络合物SnCl
,防止Fe2+的干扰,故答案为:将溶液中过量的Sn2+转化为稳定的络合物SnCl![]() ,防止Fe2+的干扰;
,防止Fe2+的干扰;
②由反应6Fe2++Cr2O![]() +14H+ = 6Fe3++2Cr3++7H2O可知,
+14H+ = 6Fe3++2Cr3++7H2O可知,![]() ,故磷酸亚铁锂电池中铁的含量为
,故磷酸亚铁锂电池中铁的含量为![]() ,故答案为:28.8%。
,故答案为:28.8%。


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】为研究废旧电池的再利用,实验室利用旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示。下列叙述错误的是
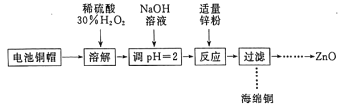
A. “溶解”操作中溶液温度不宜过高
B. 铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的氧气或H2O2
C. 与锌粉反应的离子可能为Cu2+、H+
D. “过滤”操作后,将滤液蒸发结晶、过滤、洗涤、干燥后,高温灼烧即可得纯净的ZnO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在电压为24V时进行如下实验,电解3分钟后,发现下列现象。
编号 | ① | ② | ③ |
装置 |
|
|
|
现象 | 小灯泡微弱发光,两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 | 两极均产生气泡,溶液无明显变化 | 两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 |
下列说法正确的是( )
A.①中小灯泡微亮是因为Ca(OH)2是弱电解质
B.对比①和②,白色浑浊的出现与电极材料无关
C.对比①和③,白色浑浊是由于OH-迁移到阳极使Ca(OH)2沉淀析出
D.阳极附近白色沉淀的成分可能是CaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在密闭容器内进行着某一反应,X 气体、Y 气体的物质的量随反应时间变化的曲线如右图。下列叙述中正确的是
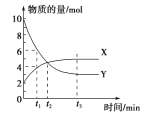
A. 反应的化学方程式为5Y![]() X B. t1 时,Y 的浓度是 X 浓度的1.5 倍
X B. t1 时,Y 的浓度是 X 浓度的1.5 倍
C. t2 时,正、逆反应速率相等 D. t3 时,逆反应速率大于正反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 1 L 0.1 mol·L-1NaClO溶液中含有的ClO-为NA
B. 1 mol Fe在1 mol Cl2中充分燃烧,转移的电子数为3NA
C. 常温常压下,32 g O2与O3的混合气体中含有的分子总数小于NA
D. 标准状况下,22.4 L HF中含有的氟原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)可表示为( )
4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)可表示为( )
A. v(NH3)=0.010mol/(L·s) B. v(O2)=0.0010mol/(L·s)
C. v(NO)=0.0010 mol/(L·s) D. v(H2O)=0.45 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是( )
A.向偏铝酸钠溶液中通入过量的CO2:2AlO![]() +CO2+3H2O=2Al(OH)3↓+CO
+CO2+3H2O=2Al(OH)3↓+CO![]()
B.向HNO2溶液中滴加酸性KMnO4溶液:5NO![]() +2MnO
+2MnO![]() +3H2O=5NO
+3H2O=5NO![]() +2Mn2++3OH-
+2Mn2++3OH-
C.向NH4HSO4溶液中滴加少量的Ba(OH)2溶液:Ba2++2OH-+NH![]() +H++SO
+H++SO![]() =BaSO4↓+NH3H2O+H2O
=BaSO4↓+NH3H2O+H2O
D.向银氨溶液中滴加乙醛溶液并水浴加热:CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO-+NH
CH3COO-+NH![]() +2Ag↓+H2O+3NH3
+2Ag↓+H2O+3NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯:6H2(g)+2CO2(g)![]() CH2===CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( )
CH2===CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( )
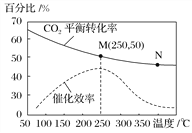
A. 该反应的逆反应为吸热反应
B. 平衡常数:KM>KN
C. 生成乙烯的速率:v(N)一定大于v(M)
D. 当温度高于250 ℃,升高温度,催化剂的催化效率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】量取8.0mL 5.0 molL-1 H2SO4溶液,加蒸馏水稀释至100mL,取两份稀释后的H2SO4溶液各25mL,分别加入等质量的Zn和Fe,相同条件下充分反应,产生氢气的体积随时间变化的曲线如图所示(氢气体积已折算成标准状况下的体积)。下列说法正确的是
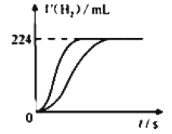
A.稀释后H2SO4溶液的物质的量浓度为0.04 molL-1
B.加入Fe的质量至少有0.56 g
C.反应过程中铁粉过量
D.金属Zn与硫酸反应转移电子数为0.01NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com