
(07年海南卷)能正确表示下列反应的离子方程式是()
A.碳酸氢钙溶液和氢氧化钠溶液混合 HCO3―+OH― = CO32―+H2O
B.醋酸钠溶液和盐酸混合 CH3COONa+H+ = CH3COOH + Na+
C.少量金属钠放入冷水中 Na+ 2H2O=Na++2OH―+H2↑
D.硫酸铜溶液和氢氧化钡溶液混合 Cu2+ + SO42― +Ba2+ + 2OH― = Cu(OH)2↓+ BaSO4↓
答案:D
解析:离子方程式正误判断
(1)看离子反应是否符合客观事实,不可主观臆造产物及反应。
(2)看“=”“ ![]() ”“↑”“↓”等是否正确。
”“↑”“↓”等是否正确。
(3)看是否漏掉离子反应。如Ba(OH)2溶液与硫酸铜溶液反应,既要写Ba2+与SO 的离子反应,又要写Cu2+与OH-的离子反应。
(4)看电荷是否守恒。
(5)看反应物或产物的配比是否正确。如稀H2SO4与Ba(OH)2溶液反应不能写成H++OH-+SO +Ba2+=BaSO4↓+H2O,
应写成2H++2OH-+SO +Ba2+=BaSO4↓+2H2O。
(6)看是否符合题设条件及要求。如“过量”“少量”“等物质的量”“适量”“任意量”以及滴加顺序等对反应方程式的影响。如 往FeBr2溶液中通入少量Cl2的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-;往FeBr2溶液中通入过量Cl2的离子方程式为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-。A选项中应产生CaCO3沉淀;B选项中CH3COONa是易溶的强电解质,应改为离子形式;C选项中电荷不守恒。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
(07年全国卷Ⅱ)能正确表示下列反应的离子方程式是()
A.醋酸钠的水解反应 CH3COO+H3O+CH3COOH+ H2O
B.碳酸氢钙与过量的NaOH溶液反应 Ca2++2HCO3+2OHCaCO3↓+ 2H2O+ CO32
C.苯酚钠溶液与二氧化碳反应 C6H5O+ CO2+ H2OC6H5OH+CO32
D.稀硝酸与过量的铁屑反应 3Fe+8H++2NO33Fe3++2NO↑+4 H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2mol/L的盐酸,与等体积水混合后pH=1
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
(07年海南卷)(9分)下表是稀硫酸与某金属反应的实验数据:
实验序号 | 金属 质量/g | 金属状态 | C(H2SO4) /mol?L-1 | V(H2SO4) /mL | 溶液温度/℃ | 金属消失的时间/s | |
反应前 | 反应后 | ||||||
1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
9 | 0.10 | 丝 | 1.1 | 50 | 20 | 44 | 40 |
分析上述数据,回答下列问题:
(1)实验4和5表明, 对反应速率有影响, 反应速率越快,能表明同一规律的实验还有 (填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号);
(3)本实验中影响反应速率的其他因素还有 ,其实验序号是 。
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
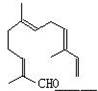
现在试剂:①KMnO4酸性溶液;②H2/Ni;③Ag(NH3)2OH;④新制Cu(OH)2, 能与该化合物中所有官能团都发生反应的试剂有()
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com