
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£¬Ļņ2LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1molCOCl2(g)·¢Éś·“Ó¦£ŗCOCl2(g)![]() Cl2(g)+CO(g)£¬·“Ó¦¹ż³ĢÖŠ²āµĆµÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
Cl2(g)+CO(g)£¬·“Ó¦¹ż³ĢÖŠ²āµĆµÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
t/s | 0 | 2 | 4 | 6 | 8 |
N(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. Ź¹ÓĆ“ß»Æ¼ĮÄܹ»øı䷓ӦĖŁĀŹ
B. “ļµ½6sŹ±£¬·“Ó¦Ķ£Ö¹£¬²»ŌŁ½ųŠŠ
C. ŌŚ8sŹ±£¬·“ӦȯĘ÷ÖŠø÷ĪļÖŹµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ
D. Éś³ÉCl2µÄĘ½¾ł·“Ó¦ĖŁĀŹ£¬0~2sÄŚĘ½¾łĖŁĀŹ±Č2~4s“ó
”¾“š°ø”æB
”¾½āĪö”æA”¢“߻ƼĮÄܹ»øı䷓ӦĖŁĀŹ£¬¹ŹAÕżČ·£»B.”¢øĆ·“Ó¦ĪŖæÉÄę·“Ó¦£¬øł¾Ż±ķøń£¬“ļµ½6sŹ±£¬Cl2µÄĮæ²»ŌŁ±ä»Æ£¬·“Ó¦²¢·ĒĶ£Ö¹£¬¶ųŹĒ“ļµ½ĮĖĘ½ŗāדĢ¬£¬±ķĆę¾²Ö¹£¬¶ÆĢ¬Ę½ŗā£¬¹ŹB“ķĪó£»C”¢ŌŚ8sŹ±£¬·“ӦȯĘ÷ÖŠø÷ĪļÖŹµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ£¬¹ŹCÕżČ·£»D”¢0~2sŹ±£¬Ōö¼ÓĮĖ0.3mol£¬2~4s£¬Ö»Ōö¼ÓĮĖ0.09mol£¬¹Ź0~2sÄŚĘ½¾łĖŁĀŹ±Č2~4s“󣬹ŹDÕżČ·£»¹ŹŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNH3ŗĶCO2ŹĒĮ½ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£®
£Ø1£©ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚ¹Ģ¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗN2+3H22NH3 £® øĆæÉÄę·“Ó¦“ļµ½»ÆŃ§Ę½ŗāµÄ±źÖ¾ŹĒ£ØĢī×ÖÄø£©£®a.3v£ØH2£©Õż=2v£ØNH3£©Äę
b£®µ„Ī»Ź±¼äÉś³ÉmmolN2µÄĶ¬Ź±ĻūŗÄ3mmolH2
c£®»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁĖꏱ¼ä±ä»Æ
d£®amol ![]() ¼ü¶ĻĮѵÄĶ¬Ź±£¬ÓŠ6amolN©H¼ü¶ĻĮŃ
¼ü¶ĻĮѵÄĶ¬Ź±£¬ÓŠ6amolN©H¼ü¶ĻĮŃ
£Ø2£©CO2ŗĶNH3æÉÓĆÓŚŗĻ³ÉÄņĖŲ£¬ŌĄķ·ÖČēĻĀĮ½²½£ŗ¢ŁŗĻ³É°±»ł¼×Ėįļ§£ŗCO2£Øg£©+2NH3£Øg£©=H2NCOONH4£Øs£©£¬”÷H=©159.47kJ/mol
¢Ś°±»ł¼×Ėįļ§·Ö½ā£ŗH2NCOONH4£Øs£©=CO£ØNH2£©2£Øs£©+H2O£Øl£©
”÷H=+28.49kJ/mol£¬Ōņ2molCO2ĶźČ«·“Ó¦ŗĻ³ÉÄņĖŲµÄ”÷H= £®
£Ø3£©×ī½üæĘѧ¼ŅĆĒŃŠÖĘ³É¹¦Ņ»ÖÖŠĀŠĶ“߻ƼĮ£¬Äܽ«CO2×Ŗ±äĪŖ¼×Ķ飮ŌŚ³£Ń¹”¢300”ę£¬CO2ÓėH2Ģå»ż±ČĪŖ1£ŗ4Ź±·“Ó¦£¬CO2×Ŗ»ÆĀŹ“ļ90%£®
¢Ł“Ė·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£»
¢ŚŅ»¶ØĢõ¼žĻĀ£¬Ä³ŠĖȤŠ”×飬ŌŚĢå»żĪŖVLµÄĆܱÕČŻĘ÷ÖŠ£¬Ä£Äā“Ė·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬£®øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ£»ÓÉĶ¼æÉÖŖÉżøßĪĀ¶Č£¬K½«£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£»300”ꏱ£¬“Ó·“Ó¦æŖŹ¼£¬µ½“ļµ½Ę½ŗā£¬ŅŌH2µÄÅØ¶Č±ä»Æ±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹŹĒ£ØÓĆnA”¢tA”¢V±ķŹ¾£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ²»ÄÜĶعżĀČĘųÓėµ„ÖŹÖ±½Ó»ÆŗĻÖĘČ”µÄŹĒ
A.FeCl2B.CuCl2C.NaClD.HCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫4mol SO2Óė2molO2·ÅČė4LµÄĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦“ļµ½Ę½ŗā£ŗ2SO2+O22SO3²āµĆĘ½ŗāŹ±»ģŗĻĪļ×ܵÄĪļÖŹµÄĮæĪŖ5mol£¬Ēó£ŗ
£Ø1£©Ę½ŗāŹ±ø÷ĪļÖŹµÄÅØ¶Č£»
£Ø2£©Ę½ŗāŹ±SO2µÄ×Ŗ»ÆĀŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æļŲ(Ga)ÓėĀĮŹōÓŚĶ¬Ö÷×åŌŖĖŲ£¬½šŹōļŲŌų±»³ĘĪŖ”°ĄąĀĮ”±£¬ĘäŃõ»ÆĪļŗĶĒāŃõ»ÆĪļ¾łĪŖĮ½ŠŌ»ÆŗĻĪļ”£¹¤ŅµÖʱø½šŹōļŲµÄĮ÷³ĢČēĻĀĶ¼ĖłŹ¾£ŗ
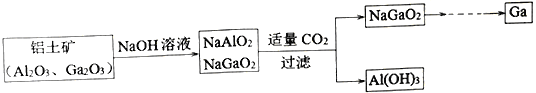
ĻĀĮŠÅŠ¶Ļ²»ŗĻĄķµÄŹĒ
A. ļŲĪŖ+3¼Ū B. ¼īŠŌ£ŗGa(OH)3>Al(OH)3
C. Ga2O3ÄÜÓėĒæĖį”¢Ēæ¼ī·“Ó¦ D. NaGaO2ÓėCO2·“Ó¦£¬ĖµĆ÷ļŲµÄ½šŹōŠŌĒæÓŚĀĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹śŌŚCO2“߻ƼÓĒāÖĘČ”ĘūÓĶ·½ĆęČ”µĆĶ»ĘĘŠŌ½ųÕ¹£¬CO2×Ŗ»Æ¹ż³ĢŹ¾ŅāĶ¼ČēĻĀ£ŗ

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©¶žŃõ»ÆĢ¼·Ö×ÓÖŠµÄ»Æѧ¼üŹĒ_________________£¬ĪļÖŹŅŅµÄ»ÆѧŹ½ŹĒ______________”£
£Ø2£©Š“³ö·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½__________________________________”£
£Ø3£©ŹµŃéŹŅ³£ÓĆ“æ¾»Ģ¼ĖįøĘÓėĻ”ŃĪĖį·“Ó¦ÖĘČ”¶žŃõ»ÆĢ¼ĘųĢ壬·“Ó¦¹ż³ĢÖŠ²śÉś¶žŃõ»ÆĢ¼µÄĖŁĀŹV(CO2) ÓėŹ±¼ä¹ŲĻµČēĻĀĶ¼£ŗ

¢ŁÓÉĶ¼Ļń·ÖĪö£¬»Æѧ·“Ó¦ĖŁĀŹ×īæģŅ»¶ĪŹĒ___________”£
¢ŚĪŖĮĖŌö“óÉĻŹö»Æѧ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬ÓūĻņČÜŅŗÖŠ¼ÓČėĻĀĮŠĪļÖŹ£¬ÄćČĻĪŖæÉŠŠµÄŹĒ_________(ĢīŠ“ŠņŗÅ)”£
A.ÕōĮóĖ® B.ĀČ»ÆÄĘČÜŅŗ C.ÅØŃĪĖį D.¼ÓČČ
£Ø4£©¶žŃõ»ÆĢ¼ÄÜÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬µ±ĒāŃõ»ÆÄĘ¹żĮæŹ±·“Ӧɜ³ÉĢ¼ĖįÄĘ£¬µ±ĒāŃõ»ÆÄĘÉŁĮæŹ±·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ”£µ±¶žŃõ»ÆĢ¼ÓėĒāŃõ»ÆÄĘ·“³ÉµÄĪļÖŹµÄĮæ±ČĪŖ2:3Ź±£¬ČÜŅŗÖŠµÄČÜÖŹŹĒ_______________”£
£Ø5£©“ÓŌ×Ó½į¹¹½Ē¶ČĖµĆ÷ŃõŌ×ӵƵē×ÓÄÜĮ¦ĒæÓŚĢ¼Ō×Ó£ŗ___________________________________”£
£Ø6£©ŌŚŅ»¶ØĢõ¼žĻĀ£¬¹¤ŅµÉĻŅ²æÉÓĆCO2ŗĻ³É¼×“¼(CH3OH)£¬Ęä»Æѧ·½³ĢŹ½ĪŖ£ŗCO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)”£ ½«a molCO2ÓėbmolH2³äČėČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬t minŹ±²āµĆ¼×“¼µÄĪļÖŹµÄĮæĪŖc mol”£¼ĘĖć0-t minÄŚCO2µÄ·“Ó¦ĖŁĀŹĪŖ_________ mol”¤L-1”¤s-1”£ [X µÄ·“Ó¦ĖŁĀŹ¦Ķ(X)=XµÄĪļÖŹµÄĮæÅØ¶Č±ä»Æ/±ä»ÆŠčŅŖµÄŹ±¼ä]
CH3OH(g)+H2O(g)”£ ½«a molCO2ÓėbmolH2³äČėČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬t minŹ±²āµĆ¼×“¼µÄĪļÖŹµÄĮæĪŖc mol”£¼ĘĖć0-t minÄŚCO2µÄ·“Ó¦ĖŁĀŹĪŖ_________ mol”¤L-1”¤s-1”£ [X µÄ·“Ó¦ĖŁĀŹ¦Ķ(X)=XµÄĪļÖŹµÄĮæÅØ¶Č±ä»Æ/±ä»ÆŠčŅŖµÄŹ±¼ä]
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ25”ꏱ£¬ĆܱÕČŻĘ÷ÖŠX£¬Y£¬ZČżÖÖĘųĢåµÄĘšŹ¼ÅضČŗĶĘ½ŗāÅضČČē±ķ£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©
ĪļÖŹ | X | Y | Z |
³õŹ¼ÅضČ/molL©1 | 0.1 | 0.2 | 0 |
Ę½ŗāÅضČ/molL©1 | 0.05 | 0.05 | 0.1 |
A.·“Ó¦“ļµ½Ę½ŗāŹ±£¬XµÄ×Ŗ»ÆĀŹĪŖ50%
B.·“Ó¦æɱķŹ¾ĪŖX+3Y2Z£¬Ę½ŗā³£ŹżĪŖ1600
C.ĘäĖūĢõ¼ž²»±äŹ±£¬Ōö“óŃ¹ĒææÉŹ¹Ę½ŗā³£ŹżŌö“ó
D.øıäĪĀ¶ČæÉŅŌøıäøĆ·“Ó¦µÄĘ½ŗā³£Źż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅ֊ijŠ©ĘųĢåµÄÖĘČ””¢ŹÕ¼Æ¼°Ī²Ęų“¦Ąķ×°ÖĆČēĶ¼ĖłŹ¾(Ź”ĀŌ¼Š³ÖŗĶ¾»»Æ×°ÖĆ)”£½öÓĆ“Ė×°ÖĆŗĶ±ķÖŠĢį¹©µÄĪļÖŹĶź³ÉĻą¹ŲŹµŃ飬×īŗĻĄķµÄŃ”ĻīŹĒ(””””)

Ń”Ļī | aÖŠµÄĪļÖŹ | bÖŠµÄĪļÖŹ | cÖŠŹÕ¼ÆµÄĘųĢå | dÖŠµÄĪļÖŹ |
A | ÅØ°±Ė® | CaO | NH3 | H2O |
B | ÅØĮņĖį | Na2SO3 | SO2 | NaOHČÜŅŗ |
C | Ļ”ŃĪĖį | ŠæĮ£ | H2 | NaOHČÜŅŗ |
D | ÅØŃĪĖį | MnO2 | Cl2 | NaOHČÜŅŗ |
A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ½āŹĶŹĀŹµµÄ·“Ó¦·½³ĢŹ½ÕżČ·µÄŹĒ£Ø £©
A.ŃĒĮņĖįÄĘĖ®ČÜŅŗĻŌ¼īŠŌ£ŗSO32©+2H2O?H2SO3+2OH©
B.SO2µÄĖ®ČÜŅŗĻŌĖįŠŌ£ŗSO2+H2O?H2SO3?2H++SO32©
C.Č¼ĆŗŹ±¼ÓČėŹÆ»ŅŹÆ¼õÉŁSO2ÅÅ·Å£ŗ2CaCO3+2SO2+O2 ![]() 2CaSO4+2CO2
2CaSO4+2CO2
D.ÅØNaOHČÜŅŗ“¦ĄķÉŁĮ涞Ńõ»ÆĮņ£ŗSO2+OH©ØTHSO3©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com