

分析 (1)根据酸的电离常数进行分析判断,电离常数越大,对应盐的水解程度越小,溶液的pH越小;
(2)根据电离常数大小分析反应的生成物;
(3)由乙酸(甲、Ka=1.8×10-5)和一氯乙酸(乙、Ka=1.4×10-3)可知,乙酸的Ka小,则乙酸的酸性弱;等浓度时酸性强的电离度大;弱酸的浓度越大,其电离度越小,以此来解答.
解答 解:(1)根据图表数据分析,电离常数:醋酸>HCN>碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,故溶液的pH为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,
故答案为:②>①>③;
(2)向NaCN溶液中通入少量CO2,由于酸性:H2CO3>HCN>HCO3-,故反应生成HCN和碳酸氢钠,不能生成二氧化碳,故反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3,
故答案为:NaCN+H2O+CO2=HCN+NaHCO3;
(3)由乙酸(甲、Ka=1.8×10-5)和一氯乙酸(乙、Ka=1.4×10-3)可知,乙酸的Ka小,则乙酸的酸性弱;
由图可知,横坐标为浓度,纵坐标为电离度,则等浓度时酸性强的电离度大,即乙的曲线在上方,可排除A、C;
弱酸的浓度越大,其电离度越小,则曲线甲、乙均随浓度的增大而下降,可排除D,显然只有B符合,
故答案为:B.
点评 本题考查盐类水解的应用,溶液中离子浓度的大小比较,弱电解质的电离,综合性较强,要注意碳酸是二元弱酸分步电离,第二部电离比HCN小,把握Ka与酸性的关系、弱酸的电离度与浓度的关系及图象分析为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
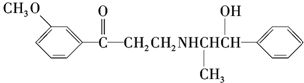
| A. | 可以在催化剂作用下和溴发生取代反应 | |
| B. | 可以和银氨溶液发生氧化反应 | |
| C. | 可以和氢溴酸发生取代反应 | |
| D. | 可以和浓硫酸与浓硝酸的混合液发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
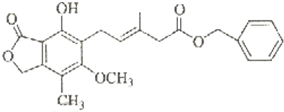
| A. | 既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 | |
| B. | 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 可以催化加氢,1 mol该物质最多可与7 mol H2反应 | |
| D. | 该化合物有4种官能团,可以使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
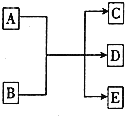 在一定条件下,物质A~E的转化关系如图所示,其中A为单质,常温下E为无色液体.
在一定条件下,物质A~E的转化关系如图所示,其中A为单质,常温下E为无色液体.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
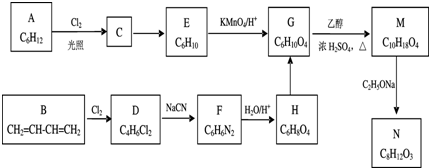
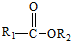 +
+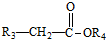 $\stackrel{C_{2}H_{5}ONa}{→}$
$\stackrel{C_{2}H_{5}ONa}{→}$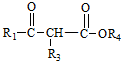 +R2OH
+R2OH .
.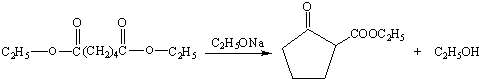 .
.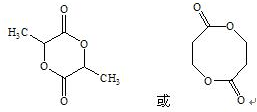 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
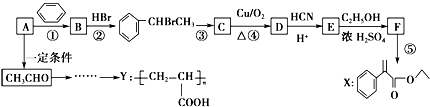
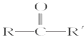 $→_{H+}^{HCN}$
$→_{H+}^{HCN}$ (R或R′可以是烃基或H原子)
(R或R′可以是烃基或H原子)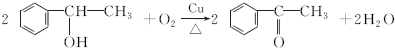 .
.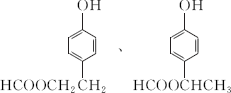 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
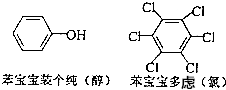 近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如右图所示).则苯酚的二氯代物同分异构体数目是( )
近期微博热传的“苯宝宝表情包”是一系列苯的衍生物配以相应的文字形成的(如右图所示).则苯酚的二氯代物同分异构体数目是( )| A. | 3 | B. | 4 | C. | 6 | D. | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作 | 现象 |
| 取适量漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝,后褪色 |
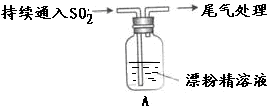 | 液面上方出现白雾; 稍后,出现浑浊,溶液变为黄绿色; 稍后,产生大量白色沉淀,黄绿色褪去 |
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com