
已知可逆反应温度为T0时,在容积固定的密闭容器中发生X(g)+Y(g) Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )
Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )
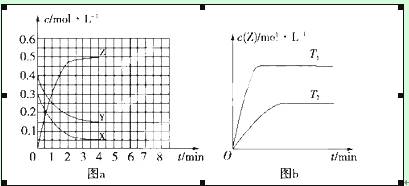
A.发生反应时,各物质的反应速率大小关系为v(X)=v(Y)=2v(Z)
B.图a中反应达到平衡时,Y的转化率为37.5%
C.T0时,该反应的平衡常数为33.3 D.该反应正反应的反应热ΔH<0
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
(1)反应Fe(s)+CO2(g)FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)FeO(s)+H2(g) ΔH2,平衡常数为K2
在不同温度时K1、K2的值如下表:
| 700 ℃ | 900 ℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
反应CO2(g)+H2(g)CO(g)+H2O(g) ΔH,平衡常数为K,则ΔH=________(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)CO(g)+H2O(g)是________反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示:

①该条件下反应的平衡常数为________;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为________mol·L-1。
②下列措施中能使平衡时 增大的是________(填序号)。
增大的是________(填序号)。
A.升高温度 B.增大压强
C.再充入一定量的CO2 D.再加入一定量铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电池的说法不正确的是 ( )。
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学将电解池工作时电子、离子流动方向及电极种类等信息表示在下图中,下列有关分析完全正确的是 ( )。

| A | B | C | D | |
| a电极 | 阳极 | 阴极 | 阳极 | 阴极 |
| d电极 | 正极 | 正极 | 负极 | 负极 |
| Q离子 | 阳离子 | 阳离子 | 阴离子 | 阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1)[2014·四川,11(4)(5)]①MnO2可作超级电容器材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是________________________________________________________________
_______________________________________________________________。
②MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时,正极的电极反应式是_________________________________________________________。
(2)[(2014·江苏,20(1)]硫化氢的转化是资源利用和环境保护的重要研究课题。
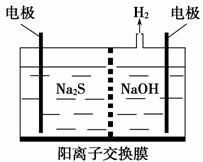
由硫化氢获得硫单质有多种方法。 将烧碱吸收H2S后的溶液加入到如上图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:
S2--2e-===S
(n-1)S+S2-===S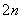
①写出电解时阴极的电极反应式:___________________________________。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成________________________________________________________________。
(3)[2014·重庆,11(4)]一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。
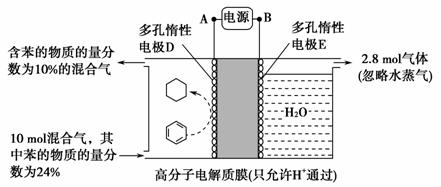
①导线中电子移动方向为________。 (用A、D表示)
②生成目标产物的电极反应式为________。
③该储氢装置的电流效率η=________(η=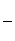 ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
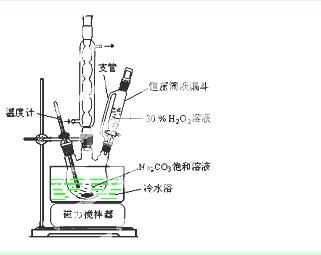
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
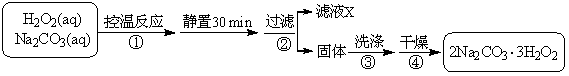
已知:主反应:2Na2CO3 (aq) + 3H2O2 (aq)  2Na2CO3·3H2O2 (s) ΔH < 0
2Na2CO3·3H2O2 (s) ΔH < 0
副反应:2H2O2 = 2H2O + O2↑,50℃时2Na2CO3·3H2O2 (s) 开始分解
请回答下列问题:
(1)步骤①的关键是控制温度,原因是 ,其措施有 、 和 。
(2)在滤液X中加入适量NaCl固体可析出过碳酸钠,原因是 。
(3)步骤③中选用无水乙醇洗涤产品的目的是 。
(4)下列物质中,会引起过碳酸钠失效的有 。
A.NaHCO3 B.MnO2 C.Na2SiO3 D.Na2SO3
(5)过碳酸钠产品中往往含有少量碳酸钠,可用重量法测定过碳酸钠的质量分数;其操作步骤:取样 品溶解→加入BaCl2溶液→过滤→洗涤→干燥→称量。需要直接测定的物理量有: 样品的质量m1g、沉淀的质量m2g(用字 母表示并注明其含义)。产品中过碳酸钠质量分数的表达式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol·L-1 Na2CO3溶液中,含CO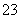 数目小于NA
数目小于NA
B.标准状况下,11.2 L O2和O3组成的混合气体含有原子数为NA
C.14 g聚乙烯与聚丙烯的混合物,含C—H键的数目为2NA
D.常温常压下,22.4 L CO2与足量Na2O2反应转移电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
2 000 K时,反应CO(g)+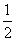 O2(g)
O2(g)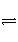
 CO2(g)的平衡常数为K,则相同温度下反应2CO2(g)
CO2(g)的平衡常数为K,则相同温度下反应2CO2(g)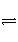
 2CO(g)+O2(g)的平衡常数K′为( )
2CO(g)+O2(g)的平衡常数K′为( )
A.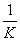 B.K2 C.
B.K2 C.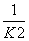 D.
D.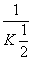
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有HCO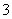 、SO
、SO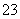 、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是( )
、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是( )
A.HCO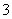 B.SO
B.SO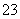 C.Cl- D.Na+
C.Cl- D.Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com