
���÷�����X��ϩ��Y���Ժϳ����������ռ�BA D����ṹ��ʽΪ��
D����ṹ��ʽΪ��
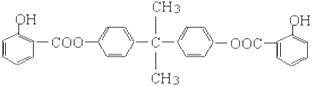
BAD�ĺϳ�·�����£�
��֪��G���ܷ���������Ӧ��B��FeCl3��Һ����ɫ��C��D�Ĺ���Ϊ�����Ȼ�(—COOH)�ķ�Ӧ��

�Իش��������⣺
��1��д���ṹ��ʽ��Y ��D ��
��2����������ȡ����Ӧ���� �� ��������ţ���
��3��1molBAD�����뺬  molNaOH����Һ��ȫ��Ӧ��
molNaOH����Һ��ȫ��Ӧ��
��4��E�ж���ͬ���칹�壬�жϷ�������Ҫ���ͬ���칹����ĿΪ �֡�
���ܷ���������Ӧ ����FeCl3��Һ����ɫ �ۺ˴Ź�������ͼ�����ĸ����շ�
��5��д����Ӧ�ںܷ͢���ʽ ��
| |
 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������������Ȼ�߷��ӻ�������ǣ� ��
A������ B����֬ C������ϩ D��������ά
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ŵIJ�ͬ�����Զ��л�����з��࣬��ָ�������л�������ŵ����ƣ����ں����ϣ�
��1��CH3COCH2COOH������
��2��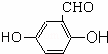 ������
������
��3��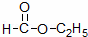 ������
������
��4��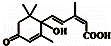 ������
������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����л���������������������ǻ��Ա�������Ӱ����ǣ� ��
A��������Һ�������� B������ ���Ҵ��У��ֱ��������ƣ����ӷ�Ӧ����
���Ҵ��У��ֱ��������ƣ����ӷ�Ӧ����
C�����ӱȱ������������Ӧ D��������������������Һ��Ӧ�������״�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��100mL NaOH��Һ��ͨ��һ������CO2���壬��ַ�Ӧ������������Һ����μ���0.2 mol/L�����ᣬ����CO2������������������֮���ϵ ����ͼ��ʾ��
����ͼ��ʾ��
�����ж���ȷ���ǣ� ��
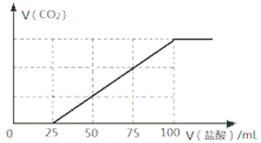
A��ԭNaOH��Һ��Ũ��Ϊ0.1 mol/L
B��ͨ��CO2�����Ϊ448 mL
C��������Һ�����ʳɷֵ����� ����֮��Ϊn(NaOH)��n(Na2CO3) = 1: 3
����֮��Ϊn(NaOH)��n(Na2CO3) = 1: 3
D��������Һ�����ʳɷֵ� ���ʵ���֮��Ϊn(NaHCO3)��n(Na2CO3) = 2: 1
���ʵ���֮��Ϊn(NaHCO3)��n(Na2CO3) = 2: 1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ�������
| �� | A�� | �к���һ����ǿ���ǿ�Ӧ�ų������� |
| �� | B�� | 1 mol����1 mol����ȫ��Ӧ�ų����������к��� |
| �� | C�� | ��ϡ��Һ�У��������кͷ�Ӧ����1 mol H2O��l��ʱ�ķ�Ӧ�Ƚ����к��� |
| �� | D�� | �ⶨ�к���ʱ����ϡ�����ϡBa��OH��2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��25�桢101kPa�����£�C��s����H2��g����CH3COOH��l����ȼ���ȷֱ�Ϊ393.5kJ/mol��285.8kJ/mol��870.3kJ/mol����2C��s��+2H2��g��+O2��g��═CH3COOH��l���ķ�Ӧ��Ϊ��������
| �� | A�� | ﹣488.3 kJ/mol | B�� | +488.3 kJ/mol |
| �� | C�� | ﹣191 kJ/mol | D�� | +191 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ڽ���Ԫ�ؼס�����Ԫ�����ڱ��е����λ�����ұ���ʾ�������ж���ȷ���ǣ�������

| �� | A�� | ԭ�Ӱ뾶������������ | B�� | ����������ԣ����������� |
| �� | C�� | �����ԣ��ף��� | D�� | �������������ף��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ȼ���кܶ࣬ƫ�����£�C2H8N2����һ�ָ���ȼ�ϣ�ȼ�ղ���������������Ϊ�������ػ�����ƶ�����������������ȷ���ǣ�������
�� A�� 6.02��1023��ƫ�����·��ӵ�����Ϊ60g
�� B�� ƫ�����µ�Ħ������Ϊ60g
�� C�� 1molƫ�����µ�����Ϊ60g/mol
�� D�� 6gƫ�����º���NA��ƫ�����·���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com