
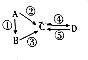
| 物质 | A | B | C | D |
| 元素种类 | 1 | 2 | 3 | 3 |
 ,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O. 分析 A、B、C、D均为短周期元素组成的常见物质,其中A是单质,
(1)若A是淡黄色固体,C是造成酸雨的主要物质,则A为S,C为SO2,B为H2S,D为SO3;
(2)若B、D两种物质均具有两性,向反应④中通入过量的温室气体,可将C转化为D,则A为Al,B为Al2O3,C为含有AlO2-,D 为Al(OH)3;
(3)若A是太阳能电池用的光伏材料,则A为Si,B、C、D所含元素均为2种,反应①、②中的反应物除A外均含有空气中的单质,则B为SiO2,C为Si3N4,D为SiF4,据此答题;
(4)若含同种元素的物质A、B、C、D均可用于杀菌消毒、漂白,其中A是黄绿色气体,则A为Cl2,C的水溶液呈酸性,则C为HClO,D的水溶液呈碱性,则D为NaClO,据此答题.
解答 解:A、B、C、D均为短周期元素组成的常见物质,其中A是单质,
(1)若A是淡黄色固体,C是造成酸雨的主要物质,则A为S,C为SO2,B为H2S,D为SO3,1molS转化为SO2时,转移电子4mol,
故答案为:H2S;4;
(2)若B、D两种物质均具有两性,向反应④中通入过量的温室气体,可将C转化为D,则A为Al,B为Al2O3,C为含有AlO2-,D 为Al(OH)3,C与过量盐酸反应的离子方程式为AlO2-+4H+=Al3++2H2O,
故答案为:AlO2-+4H+=Al3++2H2O;
(3)若A是太阳能电池用的光伏材料,则A为Si,B、C、D所含元素均为2种,反应①、②中的反应物除A外均含有空气中的单质,则B为SiO2,C为Si3N4,D为SiF4,D的一种用途为有机硅化合物的合成材料,
故答案为:SiF4;有机硅化合物的合成材料;
(4)若含同种元素的物质A、B、C、D均可用于杀菌消毒、漂白,其中A是黄绿色气体,则A为Cl2,A的电子式为 ,C的水溶液呈酸性,则C为HClO,D的水溶液呈碱性,则D为NaClO,反应A→D的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
,C的水溶液呈酸性,则C为HClO,D的水溶液呈碱性,则D为NaClO,反应A→D的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为: ;HClO;Cl2+2OH-=Cl-+ClO-+H2O.
;HClO;Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题考查无机物推断,涉及硫、铝、硅、氯等元素化合物性质及转化,难度中等,注意对基础知识的理解掌握,熟记常见元素化合知识是解题的关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 22 g 2H218O中含有的质子数为10NA | |
| B. | 标准状况下,2.24 L乙醇中含有的C-H键数目为0.5NA | |
| C. | 0.1 mol/L的NaF溶液中所含F-的数目小于0.1NA | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去0.5NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol•L-1氨水中加入少量水,溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$减少 | |
| B. | 将NH4Cl溶液从20℃升温至30℃,溶液中$\frac{c(N{H}_{4})}{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}$增大 | |
| C. | 向氢氧化钠溶液中加入醋酸至中性,溶液中$\frac{c(C{H}_{3}COO)}{c(N{a}^{+})}$=1 | |
| D. | 向含有BaSO4、BaCO3的饱和溶液中加入少量的Ba(NO3)2,溶液中的$\frac{c(S{O}_{4}^{2-})}{c(C{O}_{3}^{2-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据分散系的稳定性将其分为胶体、溶液和浊液 | |
| B. | 根据化合物在溶液中能否电离将其分为强电解质和弱电解质 | |
| C. | 根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸和多元酸 | |
| D. | 根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学和环境保护、食品营养、材料应用等密切相关.
化学和环境保护、食品营养、材料应用等密切相关. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com