
【题目】现有三组溶液:①汽油和氯化钠溶液 ②碘的CCl4溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A. 萃取、蒸发、分液 B. 分液、蒸馏、萃取
C. 分液、萃取、蒸馏 D. 蒸馏、萃取、分液
科目:高中化学 来源: 题型:
【题目】下列化合物中不可能通过化合反应制得的有( )个
①Fe(OH)3 ②FeCl2 ③FeI3 ④SO3 ⑤CuS ⑥NaHCO3
A.2个B.3个C.4个D.5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题: 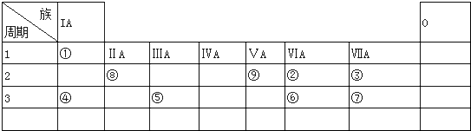
(1)周期表中元素最高正价与最低价代数和为零的是族(用族序号表示).
(2)⑥和⑦的最高价含氧酸的酸性强弱为(用酸的化学式表示).
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式;
(4)已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式 .
(5)已知W+X=Y+Z(反应需要加热,),W,X,Y,Z分别是由①②⑨三种元素形成的四种十电子粒子(W,X为离子,Y,Z为分子),写出该化学方程式 .
(6)由表中元素形成的物质可发生如图中的反应,其中B,C,G是单质,B为黄绿色气体,D溶液显碱性. 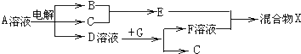
①写出D溶液与G反应的化学方程式 .
②写出检验A溶液中溶质的阴离子的方法 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法不正确的是( )
A. 1mol葡萄糖与足量的钠反应能产生2.5mol H2
B. a g某气体中含分子数为b,c g该气体在标况下的体积为(22.4bc)/(aNA)
C. 将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-) =2NA(N表示粒子数)
D. 相同质量的Na2O2和Na2S固体具有相同的阴阳离子数和质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“粗盐提纯”实验中,下列操作正确的是( )
A. 过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤
B. 蒸发到析出晶体时才需要用玻璃棒搅拌
C. 当蒸发皿中出现较多量晶体时就应停止加热
D. 待溶液蒸干后即停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有短周期元素A,B,C,D,E,
已知:①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜;
②B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍;
③E与A同周期,C,D,E三种元素形成的单质或化合物可发生如图所示的反应.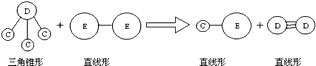
请回答下列问题:
(1)写出A元素最高价氧化物与NaOH溶液反应的离子方程式:;
(2)D元素的原子结构示意图是:;
(3)B元素与E元素的最高价氧化物的水化物的酸性强弱(用化学式表示):>;
(4)请用化学方程式表示E元素的单质在工业上的一种重要用途: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是炼铜的最主要矿物。火法冶炼黄铜矿的过程中,其中一步反应是;2Cu2O+ Cu2S![]() 6Cu+SO2。回答下列问题。
6Cu+SO2。回答下列问题。
(1)Cu+的价电子轨道表示式为__________________;Cu2O与Cu2S比较,熔点较高的是_______,原因为_____________________________________。
(2)SO2与SO3的键角相比,键角更大的是____________。将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如下图1所示。此固态SO3中S原子的杂化轨道类型是_______;该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为_________(填图中字母)。
(3)离子化合物CaC2的一种晶体结构如下图2所示。写出该物质的电子式_____。从钙离子看,属于____________堆积;一个晶胞含有的π键平均有______个。
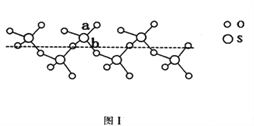
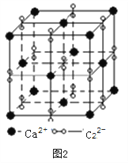

(4)奥氏体是碳溶解在γ—Fe中形成的一种间隙固溶体,无磁性,其晶胞如上图3所示,则该物质的化学式为________,若晶体密度为dg/cm3,则晶胞中最近的两个碳原子的距离为____________________ pm。(阿伏加德罗常数的值用NA表示,写出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。
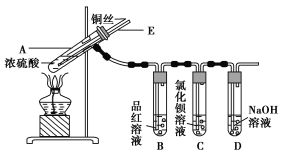
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为 。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是 。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 |
写出其中SO2表现还原性的离子反应方程式: 。
(4)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是 。
(5)实验完毕后,装置中残留的气体有毒,不能打开导管上的胶塞。为了防止该气体排入空气中污染环境,拆除装置前,应当采取的操作是 。
(6)将SO2气体通入含有n mol Na2S的溶液中,充分反应后,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体 mol(不考虑溶解的SO2)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com