
肼(N2H4)是火箭发动机的燃料,它与N2O4反应时,N2O4为氧化剂,生成氮气和水蒸气。已知:N2(g)+2O2(g)===N2O4(g) ΔH=+8.7 kJ/mol,N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534.0 kJ/mol,下列表示肼跟N2O4反应的热化学方程式,正确的是( )
A.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-542.7 kJ/mol
B.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-1 059.3 kJ/mol
C.2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g) ΔH=-1 076.7 kJ/mol
D.N2H4(g)+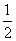 N2O4(g)===
N2O4(g)===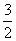 N2(g)+2H2O(
N2(g)+2H2O( g) ΔH=-1 076.7 kJ/mol
g) ΔH=-1 076.7 kJ/mol
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
下列推断正确的是( )
A.SO2和CO2都是酸性氧化物,都能与NaOH溶液反应
B.Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同
C.NO和NO2的密度都比空气大,都可以用向上排空气法收集
D.C3H8和CH3CH2OH相对分子质量相近,二者沸点也相近
查看答案和解析>>
科目:高中化学 来源: 题型:
化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下列相关说法正确的是________(填序号)。
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池
的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提上日程,其首要原因是电池外壳的金属材料需要回收
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应式可表示为
2Ni(OH)2+Cd(OH)2 Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O
已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法正确的是________(填序号)。
A.以上反应是可逆反应
B.反应环境为碱性
C.电池放电时Cd作负极
D.该电池是一种二次电池
(3)在宇宙飞船和其他航天器上经常使用的氢氧燃料电池是一种新型电源,其构造如图所示:a、b两个电极均由多孔的碳块组成,通入的氢气和氧气由孔隙中逸入,并在电极表面发生反应而放电。
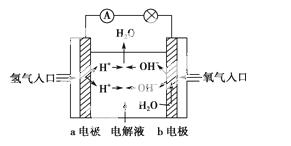
①a电极是电源的________极;
②若该电池为飞行员提供了360 kg的水,则电路中通过
了________mol电子。
(4)请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱,请画出实验装置图并写出电极反应式。
查看答案和解析>>
科目:高中化学 来源: 题型:
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①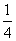 CaSO4(s)+CO(g)
CaSO4(s)+CO(g) 
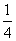 CaS(s)+CO2(g) ∆H1= —47.3kJ∙mol-1
CaS(s)+CO2(g) ∆H1= —47.3kJ∙mol-1
② CaSO4(s)+CO(g)  CaO(s)+CO2(g) +SO2(g) ∆H2= +210.5kJ∙mol-1
CaO(s)+CO2(g) +SO2(g) ∆H2= +210.5kJ∙mol-1
③ CO(g) 
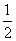 C(s)+
C(s)+ 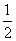 CO2(g) ∆H3= —86.2kJ∙mol-1
CO2(g) ∆H3= —86.2kJ∙mol-1
(1)反应2CaSO4(s)+7CO(g)  CaS(s)+ CaO(s)+6CO2(g)+ C(s) +SO2(
CaS(s)+ CaO(s)+6CO2(g)+ C(s) +SO2( g)的∆H=___________(用∆H1、∆H2和∆H3表示)
g)的∆H=___________(用∆H1、∆H2和∆H3表示)
( 2)反应①-③的平衡常数的对数lgK随反应温度T的变化曲线见图18,结合各反应的∆H,归纳lgK-T曲线变化规律:
2)反应①-③的平衡常数的对数lgK随反应温度T的变化曲线见图18,结合各反应的∆H,归纳lgK-T曲线变化规律:
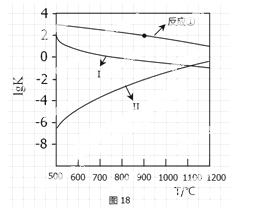
a)_______________________________;b)____________________________。
(3)向盛有CaSO4的真空恒容密闭容器中充入CO,反应①于900℃达到平衡,c平衡(CO)=8.0×10-5 mol∙L-1,计算CO的转化率(忽略副反应 ,结果保留两位有效数字)。
,结果保留两位有效数字)。
(4)为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入____________。
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生CaSO4,该反应的化学方程式为_______________;在一定条件下,CO2可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化过程,属于放热反应的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓H2SO4稀释
④固体NaOH溶于水 ⑤H2在Cl2中燃烧 ⑥食物腐败
A.②③④⑤⑥ B.②③④
C.②⑤⑥ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知R元素的某种同位素能形成化合物AmRn,其中A的化合价为+n。该化合物中一个R微粒的核外电子数为a,核内中子数为b,则该同位素的原子符号是( )
A.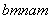 R B.
R B.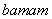 R
R
C.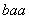 R D.
R D.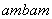 R
R
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )
| X | Y |
| Z | W |
A.若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
B.若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
C.若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
D.若四种元素中只有一种为金属,则Z与Y两者的最高价氧化物对应的水化物能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.1mol/L醋酸溶液的pH=3。将该温度下0.2 mol/L醋酸溶液和 0.2mol/L醋酸钠溶液等体积混合后,混合液的pH=4.7,下列说法正确的是( )
A.该温度下,0.0lmol/L醋酸溶液的pH=4
B.该温度下,用0.1mol/L醋酸和0.01 mol/L醋酸分别完全中和等体积0.1 mol/L的NaOH溶液,消耗两醋酸的体积比为1∶10
C.该温度下,0.01mol/L醋酸溶液中由水电离出的c(H+)=10-11mol/L
D.该温度下,0.2mol/L醋酸溶液和0.2mol/L醋酸钠溶液等体积混合后,混合液中c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.光催化还原水制氢比电解水制氢更节能环保、更经济
B.氨氮废水(含NH 及NH3)可用化学氧化法或电化学氧化法处理
及NH3)可用化学氧化法或电化学氧化法处理
C.某种化学检测技术具有极高的灵敏度,可检测到单个细胞(V≈10-12 L)内的数个目标分子,据此可推算该检测技术能测量细胞内浓度约为10-12~10-11mol·L-1的目标分子
D.向汽油中添加甲醇后,该混合燃料的热值不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com