
【题目】H2S与CO2在高温下发生反应:CO2 (g) + H2S (g) ![]() COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
COS (g) + H2O (g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。下列说法不正确的是
A. 升高温度,H2S浓度增加,表明该反应是放热反应
B. 通入CO2后,正反应速率先增大后减小
C. H2S的平衡转化率α = 4.5 %
D. 反应平衡常数K = 1/351
【答案】C
【解析】
A.升高温度,H2S浓度增加,说明平衡逆向移动,因此正反应为放热反应,故A正确;
B.通入CO2瞬间,正反应速率最大,但随着反应进行,正反应速率逐渐减小,故B正确;
C. H2S(g) + CO2(g)COS(g)+H2O(g)
起始(mol) 0.40 0.10 0 0
转化(mol) x x x x
平衡(mol) 0.40-x 0.10-x x x
反应平衡后水的物质的量分数为0.02,则![]() =0.02,x=0.01,H2S的平衡转化率α=
=0.02,x=0.01,H2S的平衡转化率α=![]() ×100%=2.5%,故C错误;
×100%=2.5%,故C错误;
D.根据C的分析,平衡浓度:c(H2S)=![]() =0.156mol/L,c(CO2)=0.036mol/L,c(COS)=c(H2O)=0.004mol/L,平衡常数K=
=0.156mol/L,c(CO2)=0.036mol/L,c(COS)=c(H2O)=0.004mol/L,平衡常数K=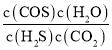 =
=![]() =
=![]() ,故D正确;
,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】盆烯是近年合成的一种有机物,它的分子结构可简化表示为![]() (其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
(其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
A. 盆烯是苯的一种同分异构体
B. 盆烯分子中所有的碳原子不可能在同一平面上
C. 盆烯是乙烯的一种同系物
D. 盆烯在一定条件下可以发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见有机物的转化关系,关于反应①~⑦的说法不正确的是( )
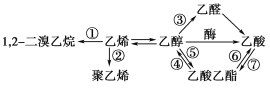
A. 只有反应③是氧化反应B. 反应①是消去反应
C. 只有反应②是加成聚合反应D. 反应④⑤⑥⑦是取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
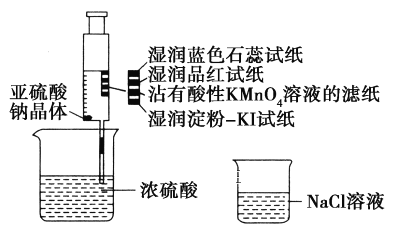
A. 蓝色石蕊试纸先变红后褪色
B. 品红试纸、沾有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性
C. 湿润淀粉-KI试纸未变蓝说明SO2的氧化性弱于I2
D. NaCl溶液可用于除去实验中多余的SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 25 ℃时0.1molL﹣1NH4Cl溶液的Kw大于100℃时0.01molL﹣1NaCl溶液的Kw
B. 常温下,pH均为3的醋酸和硫酸铝两种溶液中,由水电离出的氢离子浓度之比为1∶108
C. 根据溶液的pH与酸碱性的关系,推出pH=6.5的溶液一定显酸性
D. 室温下,将pH=2的盐酸与pH=12的氨水等体积混合,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一固体粉末,可能由Na2CO3、Na2SO4、CuSO4、NH4Cl中的一种或几种组成,为了检验它们所含的物质,做了以下实验。
①将固体溶于水,搅拌后得到无色透明溶液;②往此溶液中滴加氯化钡溶液,有白色沉淀生成;③过滤,将沉淀置于稀盐酸中,发现沉淀不溶解。
(1)试判断:固体混合物中肯定含有____________________,生成白色沉淀的化学方程式______________________________________;肯定没有_____________________________;可能含有________________________
(2)检验是否含有可能存在的物质的实验方法是:________化学方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | b | ||||||||||||||||
[ | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o |
请根据要求用元素符号或化学式回答下列问题:
(1)表中所列元素中,原子最外层有2个电子的元素为_________。
(2)画出d元素原子的结构示意图_______________________________,其气态氢化物溶于水显_____________性。(填“酸”或“碱”)
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱________>__________。
(4)表中j元素在元素周期表中的位置是______________________。
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是___________(填写化合物的化学式,下同),具有两性的是_____________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 向0.1mol/LCH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小
B. 将CH3COONa溶液从20℃升温至30℃,溶液中c(CH3COO-)/c(CH3COOH)·c(OH-)增大
C. 向盐酸中加入氨水至中性,溶液中c(NH4+)/c(Cl-)>1
D. 向AgCl、AgBr的饱和溶液中加入少量硝酸银,溶液中c(Cl-)/c(Br-)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)硫酸镍溶于过量的氨水可形成[Ni(NH3)6]SO4溶液。
①[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为_____,中心原子(离子)是____;
②SO42-中,中心原子的轨道杂化类型为_______;
③写出一种与SO42-互为等电子体的分子的化学式______;
(2)NH3极易溶于水,除因为它们都是极性分子外,还因为__________。
(3)已知H—H键能为436kJ/mol,N≡N键的键能为945kJ/mol,根据化学方程式:N2+3H2 ==2NH3 ΔH=-92.4kJ/mol,则H—N键能为____kJ/mol。
(4)下列分子既存在p-sp σ键,也存在p-p π键的是_____。
A.NH3 B.H2 C.CO2 D.C2H2
(5)根据已经掌握的共价键知识判断,键的极性N—H___O—H(“>”,“=”或“<”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com