
下列叙述正确的是( )
|
| A. | 将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42﹣)>c(NH4+) |
|
| B. | 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 |
|
| C. | pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
|
| D. | 向0.1mol•L﹣1的氨水中加入少量硫酸铵固体,则溶液中 |
考点:
酸碱混合时的定性判断及有关ph的计算.
专题:
电离平衡与溶液的pH专题.
分析:
A.溶液显示中性,氢离子与氢氧根离子浓度相等,根据电荷守恒进行判断硫酸根离子与铵根离子浓度大小;
B.醋酸为弱酸,浓度越大,电离程度越小,据此进行分析;
C.醋酸为弱电解质,溶液中部分电离出氢离子,所以两溶液混合后醋酸过量,溶液显示酸性;
D.氨水中进入硫酸铵,溶液中铵根离子浓度增大,氨水电离程度减小,一水合氨浓度增大,溶液中氢氧根离子浓度减小,则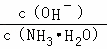 减小.
减小.
解答:
解:A.将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,则溶液中c(OH﹣)=c(H+),根据电荷守恒c(H+)+2c(SO42﹣)=c(OH﹣)+c(NH4+)可知:2c(SO42﹣)=c(NH4+),即c(SO42﹣)<c(NH4+),故A错误;
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,设电离度分别为x、y,则x×c1=10y×c2;由于醋酸浓度越大,电离程度越小,即x<y,则c1= 10c2>10c2,故B错误;
10c2>10c2,故B错误;
C.醋酸为弱酸,pH=1的醋酸溶液醋酸的浓度大于0.1mol/L,而pH=13的NaOH溶液中氢氧化钠的浓度为0.1mol/L,两溶液混合后醋酸过量,溶液显示酸性,则滴入石蕊溶液呈红色,故C正确;
D.0.1mol•L﹣1的氨水中加入少量硫酸铵固体,溶液中铵根离子浓度增大,氨水的电离平衡性质逆向移动,一水合氨浓度增大,溶液中氢氧根离子浓度减小,则溶液中 减小,故D错误;
减小,故D错误;
故选C.
点评:
本题考查了酸碱混合后的定性判断及溶液pH的计算,题目难度中等,注意掌握溶液酸碱性与溶液pH的关系,明确弱电解质在溶液中部分电离,存在电离平衡,且浓度越大,电离程度越小.


科目:高中化学 来源: 题型:
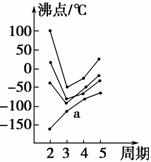 如图中每条折线表示周期表ⅣA族~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是 ( )。
如图中每条折线表示周期表ⅣA族~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是 ( )。
A.H2S B.HCl
C.PH3 D.SiH4
查看答案和解析>>
科目:高中化学 来源: 题型:
根据所学的元素周期律知识,下列说法正确的是()
A. 碱金属元素从上到下随核电荷数的增加,单质的熔沸点逐渐升高
B. 第二周期元素(除稀有气体外)从左到右随核电荷数的增加,其最高正价从+1到+7
C. Se的氢化物应该比硫化氢稳定
D. Sr的碳酸盐应该难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
某烷烃的相对分子质量为72,跟氯气发生取代反应所得的一氯取代物有3种同分异构体,这种烷烃是()
A. CH3CH2CH2CH2CH3 B. 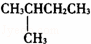
C. 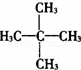 D.
D. 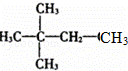
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应X(g)+3Y(g)⇌2Z(g)达到化学平衡状态的标志是( )
|
| A. | X、Y、Z的分子数比为1:3:2 |
|
| B. | 单位时间生成amolX,同时生成3a molY |
|
| C. | X、Y、Z的浓度相等 |
|
| D. | 3v正(X)=v逆(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物性质的说法正确的是( )
|
| A. | 乙烯和甲烷都可以与氯气反应 |
|
| B. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
|
| C. | 乙烯和苯都能使酸性高锰酸钾溶液褪色 |
|
| D. | 乙烯和乙烷都可以与氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某化合物有碳、氢、氧三种元素组成,其红外光谱图有C﹣H键、O﹣H键、C﹣O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式是( )
|
| A. | CH3CH2OCH3 | B. | CH3CH2CH(OH)CH3 |
|
| C. | CH3CH2CH2OH | D. | CH3CH2CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组为研究电化学原理,设计如图装置.下列叙述错误的是()
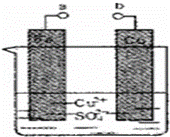
A. a和b不连接时,铁片质量会增加
B. a和b用导线连接时,正极发生的电极反应为:Cu2++2e﹣═Cu
C. 无论a和b是否连接,铁片均被腐蚀
D. a和b分别连接电源正、负极时,Fe电极发生的电极反应为:4OH﹣﹣4e﹣═2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是 ( )。
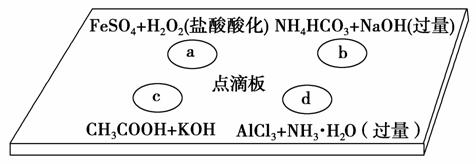
A.a反应:Fe2++2H++H2O2===Fe3++2H2O
B.b反应:HCO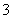 +OH-===CO
+OH-===CO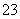 +H2O
+H2O
C.c反应:H++OH-===H2O
D.d反应:Al3++3NH3·H2O===Al(OH)3↓+3NH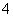
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com