
| A、大于a | B、小于a |
| C、等于a | D、无法确定 |
科目:高中化学 来源: 题型:
| A、该分子不能发生加成反应 |
| B、分子中N≡C键的键长大于C-C键的键长 |
| C、分子中含有3个σ键和4个π键 |
| D、不和氢氧化钠溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、该反应从氧化还原反应的电子转移看,与SO2+2H2S═3S+2H2O是同一反应类型 | ||||
| B、该反应中,氧元素氧化了硫元素 | ||||
C、该反应从氧化还原反应的电子转移角度看,与6NO2+8NH3
| ||||
| D、该反应中,Cu2S既是还原剂又是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酒精能使蛋白质变性,可用于杀菌消毒 |
| B、CaO能用于燃煤的脱硫 |
| C、明矾水解时产生具有吸附性的胶体粒子,可以除去水中的杂质离子 |
| D、氯气泄露时,人群应向高处疏散 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同一原子中,4S、2P、4P能级的轨道数依次增多 |
| B、3P2表示3P能级有两个轨道 |
| C、处于最低能量的原子叫做基态原子 |
| D、同一原子中,1S、2S、3S电子的能量逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)
N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )
N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )| A、减小NO2的浓度 |
| B、降低温度 |
| C、增加压强 |
| D、升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第一电离能:③>①>② |
| B、原子半径:③>②>① |
| C、电负性:③>①>② |
| D、最高正化合价:③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
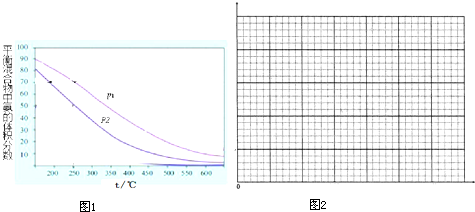
| 压强(MPa) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 氨的平衡含量(%) | ||||||
| 温度(摄氏度) | ||||||
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.1 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
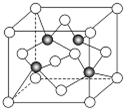 目前大量的照明材料或屏幕都使用了发光二极管(LED).市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如图.试回答:
目前大量的照明材料或屏幕都使用了发光二极管(LED).市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如图.试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com