
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( )
A.水既是氧化剂又是溶剂 B.放电时正极上有氢气生成
C.放电时OH-向正极移动 D.总反应为:2Li+2H2O === 2LiOH+H2↑
科目:高中化学 来源: 题型:
下列说法正确的是( )
①参加反应的物质的性质是影响化学反应速率的主要因素
②光是影响某些化学反应速率的外界条件之一 ③决定化学反应速率的主要因素是浓度 ④不管什么反应,增大浓度、加热、加压、使用催化剂都可以加快反应速率
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于电解质的叙述正确的是( )
A.电解质溶液的浓度越大,其导电性能一定越强
B.强酸和强碱一定是强电解质,不管其水溶液浓度的大小,都能完全电离
C.强极性共价化合物不一定都是强电解质
D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220 kJ/mol
7molH2与C3H8混合物完全燃烧,共放热5869kJ,则二者的体积比V(H2):V(C3H8)为
A.1:1 B.2:5 C.3:4 D.5:2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;B的最外层电子数为其内层电子数的3倍;A与C可形成离子化合物C3A2;D是地壳中含量最多的金属元素;E原子核外的M层中有两对成对电子;F原子核外最外层只有1个电子,其余各层电子均充满。根据以上信息,回答下列问题:(A、B、C、D、E、F用所对应的元素符号表示)
F原子的核外电子排布式为 ,A、B、C、D、E的第一电离能最小的是 。
C的氧化物的熔点远高于E的氧化物的熔点,原因是 。
比较B、E的氢化物的沸点_________。
A的最高价含氧酸根离子中,其中心原子是 杂化,E的低价氧化物的空间构型为 。
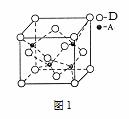
A、D形成某种化合物的晶胞结构如图1,则其化学式为 。
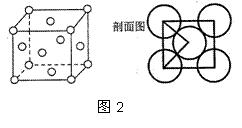
F单质的晶体的晶胞结构如图2。若F原子的半径是r cm,则F单质的密度的计算公式是 。(用NA表示阿伏伽德罗常数)

查看答案和解析>>
科目:高中化学 来源: 题型:
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
 (1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
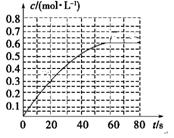
(2)298 K时,在2L的密闭容器中,发生可逆反应:2NO2(g)
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变
化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
①298k时,该反应的平衡常数为________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
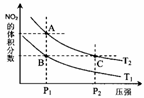 a.A、C两点的反应速率:A>C
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
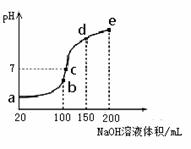 (3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是__________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是_______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X元素的阳离子和Y元素的阴离子具有相同的电子层结构,下列叙述正确的是( )
A.原子序数:X<Y B. 电负性:X<Y
C.离子半径:X>Y D.原子半径:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示(石墨仅表示出其中的一层结构):
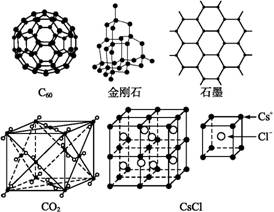
(1)C60、金刚石和石墨三者的关系是互为 。
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于 (填“原子”或“分子”)晶体,C60分子中含有双键的数目是 。
(3)晶体硅的结构跟金刚石相似,1 mol晶体硅中含有硅—硅单键的数目是 NA。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是 。
(5)观察CO2分子晶体结构的一部分,试说明每个CO2分子周围有 个与之紧邻且等距的CO2
分子;该结构单元平均占有 个CO2分子。
(6)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为 ,每个Cs+周围距离相等且次近的Cs+数目为 ,距离为 ,每个Cs+周围距离相等且第三近的Cs+数目为 ,距离为 ,每个Cs+周围紧邻且等距的Cl-数目为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是( )
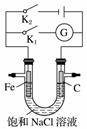
A.K1闭合,铁棒上发生的反应为2H++2e-—→H2↑
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001 mol气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com