
”¾ĢāÄæ”æ»ÆѧÓėČĖĄąÉś²ś”¢Éś»īŗĶÉē»įæɳ֊ų·¢Õ¹ĆÜĒŠĻą¹Ų”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ( )
A£®¹ā»ÆѧŃĢĪķŹĒµŖŃõ»ÆĪļŹÜ×ĻĶāĻßÕÕÉäŗóÓėæÕĘųÖŠµÄŅ»Š©Ģ¼Ēā»ÆŗĻĪļ×÷ÓĆŗóÉś³ÉµÄŅ»ÖÖÓŠ¶¾ŃĢĪķ
B£®”°ĆŗøÄĘų”±”¢”°Ćŗøĵē”±µČĒå½ąČ¼ĮĻøÄŌģ¹¤³ĢÓŠĄūÓŚ¼õÉŁĪķö²ĢģĘų
C£®ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒÓ¦ÓĆ»ÆѧŌĄķ¶Ō»·¾³ĪŪČ¾½ųŠŠÖĪĄķ
D£®ŗ½Ģģ·É»śÉĻŹ¹ÓƵÄøōČČĢÕ“ÉĶߣ¬“󶹏ĒŅŌĢ¼ĻĖĪ¬×öŌöĒæĢåµÄŠĀŠĶø“ŗĻ²ÄĮĻ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ÓĆ0.1000 mol/L NaOHČÜŅŗ·Ö±šµĪ¶Ø20.00 mL 0.1000 mol/L HClČÜŅŗŗĶ20.00 mL 0.1000 mol/L CH3COOHČÜŅŗ£¬µĆµ½2ĢõµĪ¶ØĒśĻߣ¬ČēĻĀĶ¼ĖłŹ¾”£

Ķ¼1 Ķ¼2
£Ø1£©CH3COOHµÄµēĄė·½³ĢŹ½ŹĒ £»
£Ø2£©ÓÉA”¢CµćÅŠ¶Ļ£¬µĪ¶ØHClČÜŅŗµÄĒśĻߏĒ £ØĢī”°Ķ¼1”±»ņ”°Ķ¼2”±£©£¬Ķ¼ĻńÖŠa = mL£»
£Ø3£©ÓĆNaOHČÜŅŗµĪ¶ØCH3COOHŹ±Ń”ÓĆ ×öÖøŹ¾¼Į£¬µ±V(NaOH)=10.00 mLŹ±£¬µĪ¶ØCH3COOHĖłµĆČÜŅŗÖŠµÄĪļĮĻŹŲŗćŹ½ŹĒ £»
£Ø4£©DµćĖłŹ¾ČÜŅŗÖŠc(Na+) c(CH3COO£)£ØĢī”°©”±”¢”°©”±”¢”°©”±£©£»
£Ø5£©Eµć¶ŌÓ¦µÄČÜŅŗpH©7£¬ŌŅņŹĒ £ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©£¬ČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµ±¹āŹųĶعżĻĀĮŠ·ÖÉ¢ĻµŹ±£¬ÄܲśÉś¶”“ļ¶ūŠ§Ó¦µÄŹĒ
A. ÕįĢĒČÜŅŗ B. µķ·Ū½ŗĢå C. ĘĻĢŃĢĒČÜŅŗ D. Ź³ŃĪĖ®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ½Ó“„·ØÖĘĮņĖįµÄÉś²śÖŠ£¬SO2×Ŗ»Æ³ÉSO3×Ŗ»ÆĀŹµÄ“óŠ”Ö±½Ó¾ö¶ØÉś²śŠ§ĀŹ”£Ä³ŃŠ¾æŠ”×éÓĆĻĀĶ¼×°ÖĆÄ£ÄāÉś²ś¹ż³ĢÖŠ²ā¶ØSO2×Ŗ»Æ³ÉSO3µÄ×Ŗ»ÆĀŹ”£ŅŃÖŖSO3µÄČŪµćŹĒ16.8”ę£¬·ŠµćŹĒ44.8”ę”£·¢Éś×°ÖĆÖŠĖłÉę¼°·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
Na2SO3(s)+H2SO4(75%)=Na2SO4+SO2ӟ+H2O
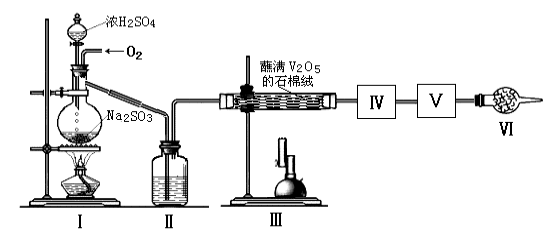
£Ø1£©¢ņÖŠµÄŹŌ¼ĮŹĒ £¬ŅĒĘ÷¢öµÄĆū³ĘĪŖ ”£
£Ø2£©øł¾ŻŹµŃéŠčŅŖ£¬Ó¦øĆŌŚ¢ō”¢¢õ“¦Į¬½ÓŗĻŹŹµÄ×°ÖĆ”£Ēė“ÓĻĀĶ¼A”«D×°ÖĆÖŠŃ”Ōń×īŹŹŗĻ×°ÖĆ²¢½«ŠņŗÅĢīČėĻĀĆęµÄæÕøńÖŠ£¬¢ō”¢¢õ“¦Į¬½ÓµÄ×°ÖĆ·Ö±šŹĒ ”¢ ”£
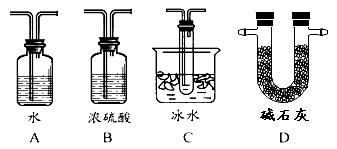
£Ø3£©ĪŖĮĖĢįøßSO2µÄ×Ŗ»ÆĀŹ£¬ŹµŃ鏱ŌŚ£ŗ¢ŁµĪ¼ÓÅØĮņĖį£»¢Ś¼ÓČČ“ß»Æ¼ĮµÄ²½ÖčÖŠ£¬Ó¦²ÉČ”µÄ²Ł×÷ŹĒĻČ_______ŗó_________(Ģī±ąŗÅ)”£
£Ø4£©ŹµŃé½įŹųŗó£¬Čē¹ū°ŃŹÕ¼ÆSO3µÄŹŌ¹Ü³ØæŚĀ¶ÖĆÓŚæÕĘųÖŠ£¬Äܹ»æ“µ½¹ÜæŚÓŠ“óĮæµÄ°×Īķ£¬²śÉś“ĖĻÖĻóµÄŌŅņŹĒ ”£
£Ø5£©ÓĆ18.9gNa2SO3·ŪÄ©Óė×ćĮæ½ĻÅصÄĮņĖį½ųŠŠ“ĖŹµŃ飬µ±·“Ó¦½įŹųŹ±£¬¼ĢŠųĶØČėO2Ņ»¶ĪŹ±¼äŗó²āµĆ×°ÖĆ¢õŌöÖŲĮĖ7.2g£¬ŌņŹµŃé²āµĆSO2µÄ×Ŗ»ÆĀŹĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČŗĶŃ¹ĒæĻĀ£¬ŗĻ³É°±·“Ó¦“ļµ½Ę½ŗāŹ±£¬ĻĀĮŠ²Ł×÷²»ÄÜŹ¹Ę½ŗā·¢ÉśŅĘ¶ÆµÄŹĒ
A£®ŗćĪĀ”¢ŗćŃ¹Ź±³äČė°±Ęų B£®ŗćĪĀ”¢ŗćČŻŹ±³äČėµŖ
C£®ŗćĪĀ”¢ŗćČŻŹ±³äČėŗ¤Ęų D£®ŗćĪĀ”¢ŗćŃ¹Ź±³äČėŗ¤Ęų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆ98%µÄÅØĮņĖį(ĘäĆܶČĪŖ1.84 g/cm3)ÅäÖĘ100 mL 1.0 mol”¤L£1Ļ”ĮņĖį,ČōŹµŃéŅĒĘ÷ÓŠ:
A”¢100mLĮæĶ²
B”¢ĶŠÅĢĢģĘ½
C”¢²£Į§°ō
D”¢50mLČŻĮæĘæ
E”¢10mLĮæĶ²
F”¢½ŗĶ·µĪ¹Ü
G”¢50mLÉÕ±
H”¢100mLČŻĮæĘæ
(1)ŠčĮæČ”ÅØĮņĖįµÄĢå»żĪŖ mL”£
(2)ŹµŃ鏱єÓƵÄŅĒĘ÷ÓŠ (Ģī×ÖÄø)
(3)ĻĀĮŠ²Ł×÷»įµ¼ÖĀĖłÅäČÜŅŗÅضČĘ«µĶµÄŹĒ________(ĢīŠņŗÅ)
¢ŁŌŚÉÕ±ÖŠ½Į°čČÜŅŗŹ±£¬ÓŠÉŁĮæŅŗĢ彦³ö
¢Ś¶ØČŻŅ”ŌČŗ󣬷¢ĻÖČÜŅŗŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ÓÖµĪ¼ÓÕōĮóĖ®ÖĮæĢ¶ČĻß
¢ŪČŻĮæĘæŹ¹ÓĆĒ°Ī“½ųŠŠøÉŌļ
¢ÜƻӊĻ“µÓČܽāŹ±ĖłÓƵÄÉÕ±ŗĶ²£Į§°ō
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»ĆܱÕČŻ»żµÄČŻĘ÷ÖŠ½ųŠŠ·“Ó¦£ŗ2SO2(g)+O2(g) ![]() 2SO3(g)”£ŅŃÖŖ·“Ó¦¹ż³Ģ֊ijŅ»Ź±æĢSO2”¢O2”¢SO3µÄÅØ¶Č·Ö±šĪŖ0.2 molL-1”¢0.1 molL-1”¢0.2 molL-1”£µ±·“Ó¦“ļĘ½ŗāŹ±£¬æÉÄÜ“ęŌŚµÄŹż¾ŻŹĒ£Ø £©
2SO3(g)”£ŅŃÖŖ·“Ó¦¹ż³Ģ֊ijŅ»Ź±æĢSO2”¢O2”¢SO3µÄÅØ¶Č·Ö±šĪŖ0.2 molL-1”¢0.1 molL-1”¢0.2 molL-1”£µ±·“Ó¦“ļĘ½ŗāŹ±£¬æÉÄÜ“ęŌŚµÄŹż¾ŻŹĒ£Ø £©
A. SO2ĪŖ0.4 molL-1£¬O2ĪŖ0.2 molL-1 B. SO2ĪŖ0.25 molL-1
C. SO2”¢SO3¾łĪŖ0.15 molL-1 D. SO3ĪŖ0.4 molL-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ( )
A£®¼×ĶéµÄ±ź×¼Č¼ÉÕČČĪŖ890.3kJ”¤mol-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCH4(g)+ 2O2 (g)=CO2(g)+2H2O(g) ”÷H£½-890.3 kJ”¤mol-1
B£®500”ę”¢30MPaĻĀ£¬½«0.5 molN2ŗĶ1.5molH2ÖĆÓŚĆܱյÄČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3(g)£¬·ÅČČ193kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2+3H2![]() 2NH3(g) ”÷H£½-38.6kJ”¤mol-1
2NH3(g) ”÷H£½-38.6kJ”¤mol-1
C£®»ī»ÆÄܵÄ×÷ÓĆŌŚÓŚŹ¹·“Ó¦Īļ»ī»Æ£¬ĖłŅŌ»Æѧ·“Ó¦µÄ»ī»ÆÄܲ»æÉÄܽӽüÓŚĮć»ņµČÓŚĮć
D£®³£ĪĀĻĀ£¬·“Ó¦C(s)+ CO2 (g)=2CO(g)²»ÄÜ×Ō·¢½ųŠŠ£¬ŌņøĆ·“Ó¦µÄ”÷H>0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢Åøł¾ŻVSEPRÄ£ŠĶÅŠ¶Ļ£¬ĻĀĮŠĪ¢Į£ÖŠĖłÓŠŌ×Ó¶¼ŌŚĶ¬Ņ»Ę½ĆęÉĻµÄŅ»×éŹĒ ”£
A”¢SO32£ŗĶNO2£ B”¢NO3£ŗĶSO3
C”¢H3O+ŗĶClO3£ D”¢PO43£ŗĶSO32£
¢ĘCaF2µÄ¾§°ūČēĶ¼ĖłŹ¾”£
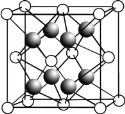
¢ŁĻĀĮŠÓŠ¹ŲCaF2µÄ±ķ“ļÕżČ·µÄŹĒ______________”£
a£®Ca2+ÓėF£¼ä½ö“ęŌŚ¾²µēĪüŅż×÷ÓĆ
b£®F£µÄĄė×Ó°ė¾¶Š”ÓŚCl££¬ŌņCaF2µÄČŪµćøßÓŚCaCl2
c£®Ņõ”¢ŃōĄė×Ó±ČĪŖ2:1µÄĄė×Ó»ÆŗĻĪļ£¬¾łÓėCaF2¾§Ģå¹¹ŠĶĻąĶ¬
d£®CaF2ÖŠµÄ»Æѧ¼üĪŖĄė×Ó¼ü£¬Ņņ“ĖCaF2ŌŚČŪȌדĢ¬ĻĀÄܵ¼µē
¢ŚCaF2ÄŃČÜÓŚĖ®£¬µ«æÉČÜÓŚŗ¬Al3+µÄČÜŅŗÖŠ£¬ŌŅņŹĒ________________________ (ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£¬ŅŃÖŖ[AlF6]3©ŌŚČÜŅŗÖŠæÉĪČ¶Ø“ęŌŚ)”£
¢Ū¾§°ūÖŠF©µÄÅäĪ»ŹżŹĒ_________£¬ÓėŅ»øöCa2+µČ¾ąĄėĒŅ×ī½üµÄCa2+ÓŠ_______øö”£
¢ĒĶ”¢ŠæĮ½ÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜ”¢µŚ¶žµēĄėÄÜČē±ķĖłŹ¾
µēĄėÄÜ/kJ”¤mol£1 | I1 | I2 |
Ķ | 746 | 1958 |
Šæ | 906 | 1733 |
¢ÜŠ“³öCuŌ×ÓŗĖĶāµē×ÓÅŲ¼Ź½ £»
¢ŻĶµÄµŚŅ»µēĄėÄÜ(I1)Š”ÓŚŠæµÄµŚŅ»µēĄėÄÜ£¬¶ųĶµÄµŚ¶žµēĄėÄÜ(I2)Č““óÓŚŠæµÄµŚ¶žµēĄėÄÜ£¬ĘäÖ÷ŅŖŌŅņŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com