
在10 L的密闭容器中进行反应N2(g) + 3H2(g)  2NH3(g),2 min末N2的物质的量 由20 mol减小到8 mol,则2 min末N2的反应速率为
2NH3(g),2 min末N2的物质的量 由20 mol减小到8 mol,则2 min末N2的反应速率为
A.1.2 mol/(L·min) B.1 mol/(L·min)
C.0.6 mol/(L·min) D.0.4 mol/(L·min)
科目:高中化学 来源: 题型:
已知有机物A的红外光谱和核磁共振氢谱如下图,下列说法错误的是 ( )
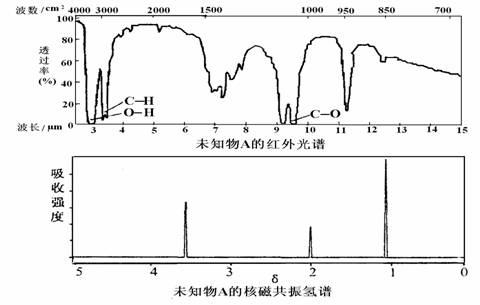
A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C3H6O,则其结构简式为CH3COCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
| 4 | ② | ④ |
(1)在这10种元素中,化学性质最不活泼的元素是 (写序号),得电子能力最强的原子是 (用元素符号表示);
(2)元素④的离子结构示意图为 ;
(3)①、⑧、⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示):
(4)写出④和⑨形成的化合物的电子式:
(5)请写出:
(ⅰ)③的单质置换出⑥的单质的化学方程式
(ⅱ)①和⑤两种元素最高价氧化物对应的水化物相互反应的化学方程式为:
(ⅲ)②和⑨两种元素最高价氧化物对应的水化物相互反应的离子方程式为:
(ⅳ)①的最高价氧化物对应水化物的水溶液与⑤的最高价氧化物反应的化学方程式为:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.离子化合物中一定含有金属元素
B.分子晶体、原子晶体中一定含有共价键,离子晶体一定含有离子键
C.气态氢化物的稳定性:NH3>PH3>AsH3
D.正四面体结构的分子中的键角一定是109°28′
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大。其相关信息如下表所示:
| X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
| Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
| Z元素的族序数是其周期数的三倍 |
| W原子的第一至第六电离能分别为:I1=578KJ·mol-1 I2=1817KJ·mol-1 I3=2745KJ·mol-1 I4=11575KJ·mol-1 I5=14830KJ·mol-1 I6=18376KJ·mol-1 |
| Q为前四周期中电负性最小的元素 |
| 元素R位于周期表的第10列 |
回答下列问题:
(1)Y元素的基态原子中未成对电子数为______;XZ分子与 Y2互为等电子体,写出XZ分子的结构式___________。
(2)W的氯化物的熔点比Q的氯化物的熔点__________(填“高”或“低”),理由是__________________________________________________。
(3)光谱证实元素W的单质与强碱性溶液反应有W(OH)4-生成,则W(OH)4-中存在(填字母)_____________。
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
(4)含有X、R和镁三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为 ;晶体中每个镁原子周围距离最近的R原子有 个。
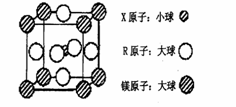
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g)+O2(g) == 2H2O(1) △H= —285.8kJ/mol
B.2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
C.2H2(g)+O2(g) == 2H2O(g) △H= —571.6 kJ/mol
D.H2(g)+ O2(g) == H2O(1) △H= —285. 8kJ/mol
O2(g) == H2O(1) △H= —285. 8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是
A.具有较高能量的分子是活化分子
B.活化分子间的碰撞一定是有效碰撞
C.反应的活化能大小不会影响化学反应速率
D.不同化学反应需要的活化能有可能差别很大
查看答案和解析>>
科目:高中化学 来源: 题型:
图187为离子交换膜法电解饱和食盐水的原理示意图,阴极由碳钢网制成,阳极由金属钛网做成(离子交换膜有只允许阳离子通过的阳离子交换膜与只允许阴离子通过的阴离子交换膜)。

图187
(1)若目标产品是从D处引出电解槽中的,则m电极应与电源的________极相连,n电极上的电极反应方程式为________________________________________________________;
精制食盐水应该从________口进入电解池中,从C处出来的液体成 分主要是______________。
分主要是______________。
(2) 当有10 mol某种离子透过L时,理论上电路中通过的电子为________NA;图中的交换膜L属于________(填“阳”或“阴”)离子交换膜,如果取消该交换膜,则溶液中 可能发生的副反应的化学方程式为_______________________________________________________。
可能发生的副反应的化学方程式为_______________________________________________________。
(3)为增大右侧电极区的导电能力,从B处引入的物质不是水而是某种物质的稀溶液,该物质可能是________。
a.NaCl b.NaOH c.Na2CO3 d.KOH
(4)受问题(2)中副反应的启示,人们开发出了一种家用“84”消毒液(有效成分为NaClO)发生器(构造如图188),在制备消毒液时,b电极上的电极反应式为________________________________________________________________________。
假设食盐最终全部转化为NaClO,写出电解总反应方程式:________________________________________________________________________
________________________________________________________________________。
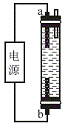
图188
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com