
【题目】磷酸铁锂电池装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。电池工作时的总反应为:LiFePO4+6C ![]() Li1-xFePO4+LixC6,则下列说法正确的是
Li1-xFePO4+LixC6,则下列说法正确的是

A. 图中聚合物隔膜是阴离子交换膜;
B. 充电时,Li+ 迁移方向是“由右向左”
C. 放电时,正极的电极反应式为LiFePO4—xe- = Li1-xFePO4 + xLi+
D. 用该电池电解精炼铜,当转移电子1.25mol时能得到精铜32g,则电子利用率为80%
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下:

已知:![]()
请回答下列问题:
(1)F的名称是 _______________,⑤的反应类型是________。 .
(2)E中的含氧官能团是________ (写名称),W的结构简式为 _________________。
(3)反应③的化学方程式是________。
(4) D发生聚合反应的化学方程式为________。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为________________。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(其他试剂任选)。
![]()
__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取SO2的反应原理为:Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
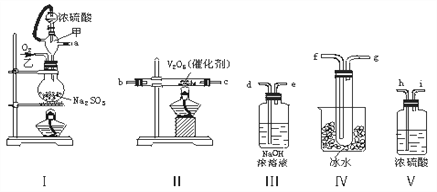
(1)装置的连接顺序(按气体左右的方向)是________________________________________________________(填各接口的编号)。
(2)实验时甲仪器的作用与原理是__________________________________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序___________________________________________________。
(4)Ⅳ处观察到的现象是____________________________________________。
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会________(填“增大”“不变”或“减小”)。
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为_______________________。(用n、m表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种溶液中含有一种卤素离子(Cl-、Br-、I-),向甲中加入淀粉溶液和氯水,则溶液变为橙色,再加丙溶液,颜色无明显变化,则甲、乙、丙中依次含有( )
A. Br-、I-、Cl-B. Br-、Cl-、I-C. I-、Br-、Cl-D. Cl-、I-、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列说法中不正确的是
A. Al2O3可用作耐火材料,硅酸钠是制备木材防火剂的原料
B. 碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜合金
C. “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
D. 绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是评价空气质量的污染物之一,主要来源于硫酸工厂的尾气和含硫燃料的燃烧。
(1)硫酸厂尾气一般采用吸收法处理。
①已知Ka(H2SO3)=1.54x10-2,Ka(HSO3-)=1.02x10-7,Kb(NH3·H2O)=1.77x10-5,将标准状况下11.2L SO2通入到2L0.5mol·L-1的氨水中,所得溶液中溶质是__________(填化学式),该溶液呈______________(填“酸”“碱”或“中”)性。
②下列关于①所得的溶液的关系正确的是_____________(填序号)。
A.2[c(NH4+)+c(NH3·H2O)]=c(SO32-)+c(HSO3-)+c(H2SO3)
B.c(NH4+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
C.c(NH4+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
D.c(NH4+)+c(OH-)=c(HSO3-)+2c(H2SO3)+c(H+)
③常温下,若用1LNaOH溶液吸收0.01mol SO2,完全吸收后溶液中c(Na+)= c(SO32-)+c(HSO3-)+ c(H2SO3),则原NaOH溶液的pH值为___________。
(2)燃煤烟气中可通过下列反应实现硫的回收:SO2(g)+2CO(g)![]() 2CO2(g)+S(l)
2CO2(g)+S(l)
①该反应的平衡常数表达式是____________。
②恒温恒压下,5分钟时,反应到达平衡,气体密度减小16g·L-1,则0-5分钟内CO的反应速率是__________,若升高温度气体的密度增加,则该反应的△H__________0(填“>”或“<”)。
③下列措施,既能提高该反应的反应速率,又能提高SO2的吸收率的是__________(填序号)。
A. 加压 B.增加SO2的浓度
B. 升高温度 D.移走产物
(3)SO2还能被多种物质吸收。
①写出SO2与Ba(NO3)2溶液反应的离子方程式:_______________。
②如果用含等物质的量溶质的下列个溶液分别吸收SO2,则理论吸收量由多到少的顺序是__________(用序号排序)。
A. H2S B.Na2SO3
C.BaCl2 D.酸性KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢吡格雷是一种血小板聚集抑制剂,该药物以2—氯苯甲醛为原料的合成路线如下

(1)A中含有的官能团名称为_________________________。其中1mol有机物A的含氧官能团含有的共用电子对数目为______NA。
(2)C→D的反应类型为_________________ ,有机反应物X的名称为______________。
(3)分子C在一定条件下生成一种含有3个六元环的产物的结构简式为_____________。
(4)写出Y在NaOH醇溶液加热条件下发生反应的化学反应方程式______________。
(5)同时满足下列两个条件的B的同分异构体共有_____种(不包括B,不考虑立体异构)
①与B含有相同的官能团;②苯环上的取代基不超过2个。
(6)已知:![]() ,则仅以甲醇、乙醇为有机原料制备
,则仅以甲醇、乙醇为有机原料制备
![]() 的合成路线流程图为______________________________________。
的合成路线流程图为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有碳、二氧化碳、氧化铁、石灰水、稀硫酸和纯碱溶液等6种物质。

①除稀硫酸外,试分别将其他物质的化学式填入如图相应的5个圆圈内,使每个圆圈内的物质都能与相邻物质发生反应。
②用化学方程式将它们与相邻物质间发生的反应表示出来:
_____________________________;
_____________________________;
_____________________________;
_____________________________;
_____________________________;
_____________________________。
(2)以下表示的是碳及其化合物之间的转化关系:
C![]() CO2
CO2![]() H2CO3
H2CO3![]() CaCO3
CaCO3![]() CO2
CO2
其中涉及的基本反应类型依次为_________、__________、__________、__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com