
| A. | PCl5 | B. | BF3 | C. | BeCl2 | D. | NaClO |
分析 A.五氯化磷中,P原子最外层电子数为5+5=10;
B.BF3中B元素化合价为+3,B原子最外层电子数为3,该化合物中B最外层含有电子数为3+3=6;
C.BeCl2中Be原子化合价为+2价,Be原子最外层电子数为2,则该化合物中Be的最外层电子数为2+2=4;
D.根据钠离子、氯离子和氧离子的离子结构示意图分析.
解答 解:A.PCl5中P元素化合价为+5价,P原子最外层电子数是5,5+5=10,则P原子不满足8电子结构,故A错误;
B.BF3中B元素化合价为+3,B原子最外层电子数为3,所以3+3=6,B原子不满足8电子结构,故B错误;
C.BeCl2中Be原子化合价为+2价,Be原子最外层电子数是2,2+2=4,所以Be原子不满足8电子结构,故C错误;
D.NaClO中,钠离子、氯离子和氧离子的离子结构示意图分别为: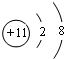 、
、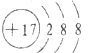 、
、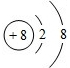 ,最外层都满足8电子稳定结构,故D正确;
,最外层都满足8电子稳定结构,故D正确;
故选D.
点评 本题考查原子核外电子排布,题目难度不大,明确共价化合物中元素化合价绝对值+元素原子的最外层电子层=8时该元素原子满足8电子结构是关键,注意掌握原子核外电子排布规律,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
| 实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
| 体积/mL | 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | |||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$互为同素异形体 | |
| B. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$电子数相同 | |
| C. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$分别含有44和46个中子 | |
| D. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有元素中居第一位 | |
| B. | 硅的化学性质不活泼,在常温下不与任何物质反应 | |
| C. | 硅在电子工业中是最重要的半导体材料 | |
| D. | 硅的性质很稳定,能以单质的形式存在于自然界中 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径:R<Z<Y | B. | 简单氢化物的热稳定性:R>Y | ||
| C. | R与Y只能形成一种化合物 | D. | 最高价氧化物的水化物酸性:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
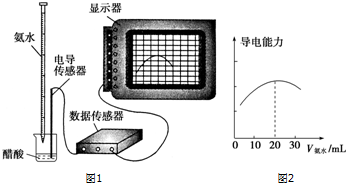
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.5g | B. | 10.5g | C. | 13.2g | D. | 24.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇代替汽油作燃料,污染小,更环保 | |
| B. | 1mol 乙醇燃烧生成3mol水 | |
| C. | 1mol 乙醇与足量Na反应生成0.5 mol H2 | |
| D. | 乙醇可以制饮料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com