
分析 (1)N原子最外层电子数是5个电子,2个电子位于2s能级、3个电子位于2p能级;O元素基态原子核外有两个未成对电子;
(2)同一周期元素,元素第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素;
(3)氨气分子中N原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断空间构型;肼分子中每个N原子价层电子对个数是4,根据价层电子对互斥理论判断N原子杂化方式;
N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内离子键、配位键和共价键;
(4)氢键键能介于化学键和分子间作用力之间;
(5)水合氢离子中O原子价层电子对个数是4,根据价层电子对互斥理论判断O原子杂化类型;孤电子对间的排斥力大于孤电子对和共用电子对之间的排斥力;
(6)CaO是面心立方晶胞,其结构和NaCl相似,则该晶胞中钙离子、氧离子个数都是4,晶胞体积=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$.
解答 解:(1)N原子最外层电子数是5个电子,2个电子位于2s能级、3个电子位于2p能级,所以其价电子排布式为2s22p3;O元素基态原子核外有两个未成对电子,
故答案为:2s22p3;2;
(2)同一周期元素,元素第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,N元素位于第VA族,所以这三种元素第一电离能大小顺序是N>O>C,故答案为:N>O>C;
(3)氨气分子中N原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论知空间构型为三角锥形;肼分子中每个N原子价层电子对个数是4,根据价层电子对互斥理论知N原子杂化方式为sp3,
N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内离子键、配位键和共价键,不存在范德华力,
故答案为:三角锥形;sp3;d;
(4)氢键键能介于化学键和分子间作用力之间,化学键键能最大,所以H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、范德华力,
故答案为:O-H键、氢键、范德华力;
(5)水合氢离子中O原子价层电子对个数是4,根据价层电子对互斥理论知O原子杂化类型为sp3;孤电子对间的排斥力大于孤电子对和共用电子对之间的排斥力,H2O中O原子有2对孤对电子,H3O+只有1对孤对电子,排斥力较小,所以H3O+中H-O-H键角比H2O中H-O-H键角大,
故答案为:sp3;H2O中O原子有2对孤对电子,H3O+只有1对孤对电子,排斥力较小;
(6)CaO是面心立方晶胞,其结构和NaCl相似,则该晶胞中钙离子、氧离子个数都是4,晶胞体积=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$=$\frac{\frac{56}{{N}_{A}}×4}{a}$cm3=$\frac{224}{{a{N_A}}}$cm3,
故答案为:$\frac{224}{{a{N_A}}}$.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、原子杂化方式判断、微粒空间构型判断、氢键等知识点,利用价层电子对互斥理论、构造原理等知识解答即可,难点是晶胞计算,注意氢键不是化学键,为分子间作用力.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 全氟丙烷的电子式为: | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 全氟丙烷分子中既有极性键又有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、D2和T2互称为同素异形体 | B. | 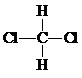 和 和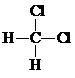 互称为同分异构体 互称为同分异构体 | ||
| C. | 35Cl和37Cl 互称为同位素 | D. | C2H4与C4H8一定能互称为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y在化合物中显+3价 | |
| B. | X与W只能形成一种化合物 | |
| C. | W的简单氢化物稳定性比Z的强 | |
| D. | X的最高价氧化物对应的水化物碱性比Y的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 );下列试剂能与甲反应而褪色的是AC(填标号)
);下列试剂能与甲反应而褪色的是AC(填标号)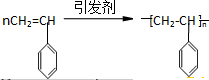 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 △H=-116kJ•mol-1
△H=-116kJ•mol-1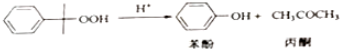 △H=-253k•mol-1
△H=-253k•mol-1
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 异丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com