
现有等物质的量的铜和银的混合物17.2 g,与50.0 mL
的浓硝酸恰好完全反应,
产生气体4.48 L(标准状况),则下列说法正确的是
A.产生的气体是0.2 mol NO2
B.硝酸的物质的量浓度为12 mol·L-1
C.反应中被还原和未被还原的硝酸物质的量之比为3∶2
D.要使产生的气体恰好完全被水吸收需要通入氧气0.075 mol
【知识点】本题考查氧化还原反应及相关计算的相关知识
【答案解析】D 解析:根据题意条件等物质的量的铜和银的混合物17.2 g,64n+108n=17.2可计算得n=0.1mol,则反应中Cu失去的电子为0.2mol,Ag失去的电子为0.1mol,硝酸所得到的电子为0.3mol,若气体为NO2则根据得失电子守恒可知NO2为0.3mol,所以A错误。根据溶液中电荷守恒可知NO3-为0.3mol,HNO3发生还原反应产生气体为0.2mol所以总的硝酸为0.5mol其浓度为0.5mol/0.05L=10mol/L, 反应中被还原和未被还原的硝酸物质的量之比为2∶3,所以BC错误。D.要使产生的气体恰好完全被水吸收,即使氮氧化物又氧化成硝酸,则失去的电子任为0.3mol,则需要0.075molO2.
【思路点拨】本题抓住氧化还原反应中电子得失守恒和质量守恒及电荷守恒三个守恒关系即可解答。难度较大。


科目:高中化学 来源: 题型:
已知氧化性Ag+>Fe3+,将铁粉投入到盛Cu2+、Ag+、Fe3+的溶液中,反应完毕时,若烧杯底部有铁粉剩余,溶液中一定不存在的金属离子是__________;若烧杯中无铁粉剩余,则溶液中一定含有的金属离子是____________;若溶液中不含Cu2+,则一定不含有的金属离子是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在溶液中能大量共存,且溶液为无色透明的离子组是
A.K+、Cu2+、Na+、Cl- B. K+、NO3-、Na+、CO32-
C. H+、NO3-、Na+、HCO3- D.Ag+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氯的说法正确的是
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.若1735Cl、1737Cl为不同的核素,有不同的化学性质
C.实验室制备Cl2,可用排饱和食盐水法收集
D.1.12 LCl2含有1.7NA个质子(NA 表示阿伏伽德罗常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数。下列叙述正确的是 ( )
A.1mol甲醇中含有C-H键的数目为4NA
B.标准状况下,2.24L已烷含有分子的数目为0.1NA
C.12克金刚石中含有的共价键数目为2NA
D.1 mol 甲基所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验Ⅰ:反应产物的定性探究。
实验装置如图所示:(固定装置已略去)

(1)A中反应的化学方程式为 。
(2)F烧杯中的溶液通常是 。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是
。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
实验Ⅱ:反应产物的定量探究
(6)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1:
| 硫酸/mol·L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
资料2:X-射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。仅由上述资料可得出的正确结论是 __。
a.铜与浓硫酸反应时所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免最后产物中出现黑色物质
c.该反应发生的条件之一是硫酸浓度≥15 mol/L
d.硫酸浓度越大,黑色物质越快出现、越难消失
(7)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量KI溶液振荡,以淀粉溶液为指示剂,用b mol/L Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为 _。(已知:2Cu2++4I-===2CuI+I2,2S2O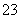 +I2===S4O
+I2===S4O +2I-)
+2I-)
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶
液中各种离子的物质的量变化如图所示。有关说法不正确的是( )
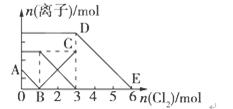
A.线段BC代表Fe3+物质的量的变化情况
B.原混合溶液中n(FeBr2)=3mol
C.当通入2molCl2时,溶液中已发生的离子反应为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中n(Fe2+):n(I-):n(Br-)=3∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2===2 Ag2S +2H2O,其中H2S是
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂就可将AgNO3、KSCN、稀H2SO4、NaOH四种无色溶液区分开来,这种试剂是( )
A.BaCl2溶液 B.FeCl2溶液
C.FeCl3溶液 D.Fe(NO3)3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com