
【题目】下列物质对水的电离平衡无影响的是:
A. KNO3 B. NH3 C. Na D. H2SO4
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
(1)实验一:取等物质的量浓度等体积H2O2溶液分别进行下列实验,实验报告如下表所示。

试回答:
①实验1、2研究的是__________________________对H2O2分解速率的影响。
②实验2、3的目的是_______________________________________________。
(2)实验二:经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

① 定性分析:如图甲可通过观察________________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________________________。
②定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是__________________________________。
(3)实验三:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显但不久突然褪色,反应速率明显加快。
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____________________的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_________。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在C(s)+CO2(g)=2CO(g)反应中,可使反应速率增大的措施是
①增大压强 ②增加炭的量 ③通入CO2 ④恒压下充入N2 ⑤恒容下充入N2 ⑥升温
A. ①③④ B. ①③⑥ C. ②④⑥ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在标况下的四种气体①6.72LCH4 ②3.01×1023个HCl分子 ③13.6克H2S④0.2molNH3用相应的序号填写下列空白:
(1)体积最大的是;
(2)原子数最多的是;
(3)质量最小的是;
(4)含氢原子数最少的是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化学方程式书写正确的是( )
A. CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
B. H2C=CH2+Br2→CH3CHBr2
C. 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D. CH3CH2OH+CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。
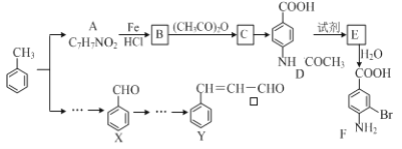
已知:①![]()
![]()
![]()
②![]()
③CH3COOH+CH3COOH→(CH3CO)2O+H2O
请回答下列问题:
(1)下列有关F的说法正确的是______________。
A.分子式是C7H7NO2Br B.F即能与HCl又能与NaOH应生成盐
C.能发生取代反应和缩聚反应 D.1 mol的 F最多可以和2 mol NaOH反应
(2)C→ D的反应类型是 _____。
(3)在合成F的过程中,B→C步骤不能省略,理由是_____________________。
(4)D→E反应所需的试剂是 ___________________。
(5)写出同时符合下列条件的A的同分异构体的结构简式(写出其中1个)_________________。
①苯环上只有两种不同化学环境的氢原子②分子中含有-CHO
(6)利用已知信息,以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。___________ 注:合成路线的书写格式参照如下示例流程图:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签部分内容。据此判断,下列说法正确的是( )

A. 1 mol Al 与足量的该硫酸产生2 g氢气
B. 配制 240 mL 4.6 mol/L 的稀硫酸需取该硫酸 40 mL
C. 洗净的锥形瓶和容量瓶可以放进烘箱中烘干
D. 该硫酸与等质量的水混合后所得溶液的物质的量浓度小于9.2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com