
| A. | 液化石油气和天然气的主要成分都是甲烷 | |
| B. | 糖类、脂类、蛋白质都属于天然高分子化合物 | |
| C. | 汽油、煤油、植物油均为含碳氢氧三种元素的化合物 | |
| D. | 误服重金属盐,立即服用牛奶或豆浆可解毒 |
分析 A.天然气的主要成分为甲烷,而液化石油气的主要成分为由丙烷、丁烷、丙烯、丁烯等;
B.根据天然有机高分子材料,首先是天然其次要求是高分子进行解答;
C.根据汽油和煤油属于烃的混合物进行判断;
D.重金属盐能够使得人体内蛋白质发生变性.
解答 解:A.液化石油气的主要成分为由丙烷、丁烷、丙烯、丁烯等,不是甲烷,故A错误;
B.油脂相对分子质量较小,不属于高分子化合物,故B错误;
C.汽油、煤油属于烃的混合物,只含C、H两种元素,植物油是高级脂肪酸与甘油形成的酯,含有C、H、O三种元素,故C错误;
D.重金属盐能够使得人体内蛋白质发生变性,重金属中毒时喝大量牛奶、蛋清或生豆浆能够有效解毒,故D正确.
故选D.
点评 本题考查了有机物的组成、结构和性质,侧重于基础知识的考查,题目把握常见有机物的性质,题目难度不大.


科目:高中化学 来源: 题型:填空题
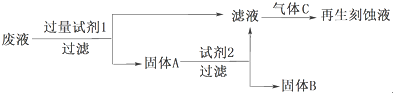
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4H是共价化合物 | B. | NH4H溶于水,所形成的溶液显碱性 | ||
| C. | NH4H与水反应时,水作还原剂 | D. | NH4H中的H元素只有一种化合价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

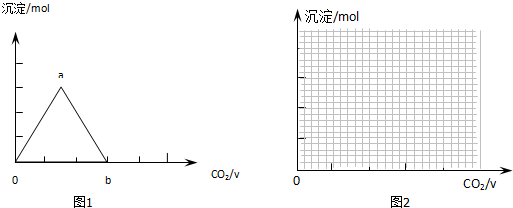
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
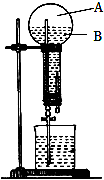 如图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B,请根据实验内容按要求填空:
如图是做过氨气溶于水的喷泉实验装置,实验完成后烧瓶里的空间被分为两个部分:A和B,请根据实验内容按要求填空: NH4++OH-(用离子方程式表示);
NH4++OH-(用离子方程式表示);查看答案和解析>>
科目:高中化学 来源: 题型:解答题
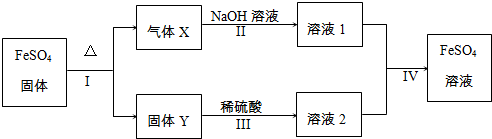
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸钙溶液中通入过量二氧化碳 Ca2++2C1O+H2O+CO2=CaCO3↓+2HClO | |
| B. | 硫酸亚铁溶液中加入过氧化氢溶液 Fe2++2H2O2+4H+=Fe3++4H2O | |
| C. | 用氨水吸收少量二氧化硫 NH3•H2O+SO2=NH4++HSO3- | |
| D. | 硝酸铁溶液中加入过量氨水 Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水土流失 | |
| B. | 汉江流域农业生产中长期使用农药 | |
| C. | 生活废水大量排入汉江,使水质富营养化 | |
| D. | 有毒的废水大量排入汉江 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com