
”¾ĢāÄæ”æijĪĀ¶ČŹ±£¬Ā±»ÆŅų(AgX£¬X£½Cl£¬Br£¬I)µÄ3ĢõČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£¬AgCl£¬AgBr£¬AgIµÄKspŅĄ“Ī¼õŠ””£ŅŃÖŖpAg£½£lgc(Ag£«)£¬pX£½£lgc(X£)£¬ĄūÓĆpX”ŖpAgµÄ×ų±źĻµæɱķŹ¾³öAgXµÄČܶȻżÓėČÜŅŗÖŠµÄc(Ag£«)ŗĶc(X£)µÄĻą»„¹ŲĻµ”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
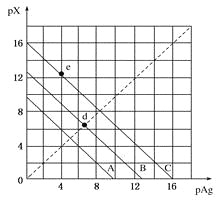
A.eµć±ķŹ¾ÓɹżĮæµÄKIÓėAgNO3·“Ó¦²śÉśAgI³Įµķ
B.AĻߏĒAgClµÄČܽāĘ½ŗāĒśĻߣ¬CĻߏĒAgIµÄČܽāĘ½ŗāĒśĻß
C.dµćŹĒŌŚĖ®ÖŠ¼ÓČė×ćĮæµÄAgBrŠĪ³ÉµÄ±„ŗĶČÜŅŗ
D.×ų±źµć£Ø8£¬4£©ŠĪ³ÉµÄČÜŅŗŹĒAgClµÄ²»±„ŗĶČÜŅŗ
”¾“š°ø”æA
”¾½āĪö”æ
AgCl£¬AgBr£¬AgIµÄKspŅĄ“Ī¼õŠ”£¬ŌņŌŚŅųĄė×ÓÅضČĻąµČµÄĢõ¼žĻĀ£¬µā»ÆŅųÖŠµāĄė×ÓµÄÅضČ×īŠ”£¬ŌņpX×ī“ó£¬ĖłŅŌĒśĻßC±ķŹ¾µā»ÆŅų£¬B±ķŹ¾äå»ÆŅų£¬A±ķŹ¾ĀČ»ÆŅųµÄČܽāĘ½ŗāĒśĻß”£
A£®eµćŌŚµā»ÆŅųµÄČܽāĘ½ŗāÉĻ£¬Ć»ÓŠAgI³Įµķ²śÉś£¬A“ķĪó£»
B£®øł¾ŻŅŌÉĻ·ÖĪöæÉÖŖAĻߏĒAgClµÄČܽāĘ½ŗāĒśĻߣ¬CĻߏĒAgIµÄČܽāĘ½ŗāĒśĻߣ¬BÕżČ·£»
C£®dµćŌŚäå»ÆŅųµÄČܽāĘ½ŗāĒśĻßÉĻ£¬Ōņ±ķŹ¾ŌŚĖ®ÖŠ¼ÓČė×ćĮæµÄAgBrŠĪ³ÉµÄ±„ŗĶČÜŅŗ£¬CÕżČ·£»
D£®×ų±źµć£Ø8£¬4£©ŌŚĀČ»ÆŅųµÄČܽāĘ½ŗāĒśĻßµÄÉĻ·½£¬ŌņŠĪ³ÉµÄČÜŅŗŹĒAgClµÄ²»±„ŗĶČÜŅŗ£¬DÕżČ·£¬
“š°øŃ”A”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉč NA ±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A.±ź×¼×“æöĻĀ£¬22.4L CCl4 ŗ¬ÓŠµÄŌ×ÓŹżĪŖ 5NA
B.1.8g µÄ NH4+ÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖ NA
C.³£ĪĀ³£Ń¹ĻĀ£¬32 g O2 ŗĶ O3 µÄ»ģŗĻĘųĢåÖŠĖłŗ¬Ō×ÓŹżĪŖ 1.5 NA
D.7.1g Cl2 ČÜÓŚĖ®£¬×ŖŅʵē×ÓŹżÄæĪŖ 0.1NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹĀŹµ²»ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶµÄŹĒ
A. ŠĀÖʵÄĀČĖ®ŌŚ¹āÕÕĢõ¼žĻĀŃÕÉ«±äĒ³
B. ŗĻ³É°±¹¤ŅµÖŠŹ¹ÓĆĢś“„Ć½×÷“߻ƼĮ
C. ŗģ×ŲÉ«µÄNO2ĘųĢ壬¼ÓŃ¹ŗóŃÕÉ«ĻȱäÉīŗó±äĒ³
D. ¹¤ŅµÉś²śĮņĖįµÄ¹ż³ĢÖŠ£¬ĶØČė¹żĮæµÄæÕĘųŅŌĢįø߶žŃõ»ÆĮņµÄ×Ŗ»ÆĀŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ298KŹ±£¬Ä³¼īMOHµÄµēĄėĘ½ŗā³£ŹżKb=1.0”Į10-5£»µēĄė¶Ča=![]() ”£ŌŚ20.00mL0.1000mol/LMOHČÜŅŗÖŠµĪ¼Ó0.10mol/LŃĪĖį£¬²āµĆČÜŅŗµÄpH”¢ĪĀ¶ČÓėĖł¼ÓŃĪĖįµÄĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
”£ŌŚ20.00mL0.1000mol/LMOHČÜŅŗÖŠµĪ¼Ó0.10mol/LŃĪĖį£¬²āµĆČÜŅŗµÄpH”¢ĪĀ¶ČÓėĖł¼ÓŃĪĖįµÄĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
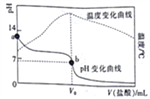
A. aµć¶ŌÓ¦µÄČÜŅŗÖŠ:c(OH-)=(M+)+<(H+)
B. bµć¶ŌÓ¦µÄV”£=20.00mL
C. 298KŹ±£¬0.1000mol/LMOHČÜŅŗÖŠ£¬MOHµÄµēĄė¶Ča=1%
D. 298KŹ±£¬½«0.1molMOHŗĶ0.1moMClČÜÓŚĖ®ÅäÖĘ³É1L»ģŗĻČÜŅŗ£¬ČÜŅŗµÄpH>9
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾ŹĒĢ¼ĖįøĘ(CaCO3)ŌŚ25 ”ęŗĶ100 ”ęĮ½ÖÖĒéæöĻĀ£¬ŌŚĖ®ÖŠµÄČܽāĘ½ŗāĒśĻß”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ

A. CaCO3(s)![]() Ca2+(aq)+ CO32£(aq) ¦¤H<0
Ca2+(aq)+ CO32£(aq) ¦¤H<0
B. a”¢b”¢c”¢dĖĵć¶ŌÓ¦µÄČܶȻżKspĻąµČ
C. ĪĀ¶Č²»±ä£¬Õō·¢Ė®£¬æÉŹ¹ČÜŅŗÓÉaµć±äµ½cµć
D. 25 ”ꏱ£¬CaCO3µÄKsp=2.8”Į10-9
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹĀŹµÖŠ£¬²»ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶµÄŹĒ
A. øÖĢśŌŚ³±ŹŖµÄæÕĘųÖŠČŻŅ×ÉśŠā
B. æŖĘōĘ”¾Ęŗó£¬ĘæÖŠĀķÉĻ·ŗĘš“óĮæÅŻÄ
C. ŹµŃéŹŅÖŠ³£ÓĆÅű„ŗĶŹ³ŃĪĖ®µÄ·½·ØŹÕ¼ÆĀČĘų
D. ¹¤ŅµÉś²śĮņĖįµÄ¹ż³ĢÖŠŹ¹ÓĆ¹żĮæµÄæÕĘųŅŌĢįø߶žŃõ»ÆĮņµÄĄūÓĆĀŹ£Ø2SO2+O2![]() 2SO3£©
2SO3£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹŅĪĀŹ±£¬Ļņ20mL 0.1mol/LµÄ“×ĖįČÜŅŗÖŠ²»¶ĻµĪ¼Ó0.1mol/LµÄNaOHČÜŅŗ£¬ČÜŅŗµÄpH±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ŌŚµĪ¶Ø¹ż³ĢÖŠ£¬ĻĀĮŠ¹ŲÓŚČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµµÄĆčŹö²»ÕżČ·µÄŹĒ
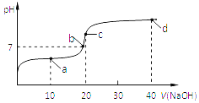
A. aµćŹ±£ŗc(CH3COO£)£¾c(Na+)£¾c(CH3COOH)£¾c(H+)£¾c(OH£)
B. bµćŹ±£ŗc(Na+) = c(CH3COO£)
C. cµćŹ±£ŗc(OH£) =c(CH3COOH) + c(H+)
D. dµćŹ±£ŗc(Na+)£¾c(CH3COO£)£¾c(OH£)£¾c(H+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢E”¢FĮłÖÖŌŖĖŲ£¬ĖüĆĒµÄŗĖµēŗÉŹż¾łŠ”ÓŚ18£¬ĒŅŌ×ÓŠņŹżÖš½„Ōö“ó”£ŅŃÖŖ£ŗA”¢C”¢FČżÖÖŌ×ÓµÄ×īĶā²ć¹²ÓŠ11øöµē×Ó£¬ĒŅÕāČżÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖ®¼äĮ½Į½½ŌÄÜ·“Ó¦£¬¾łÉś³ÉŃĪŗĶĖ®”£DŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹż±Č“ĪĶā²ćµē×ÓŹżÉŁ4øö£¬EŌŖĖŲŌ×ӵēĪĶā²ćµē×ÓŹż±Č×īĶā²ćµē×ÓŹż¶ą3øö”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öDµÄŌŖĖŲ·ūŗÅ_____________£¬EµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ·Ö×ÓŹ½_____________”£
£Ø2£©»³öBŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼_____________”£
£Ø3£©Čō¹¹³ÉFŌŖĖŲµÄŅ»ÖÖŗĖĖŲµÄÖŠ×ÓŹżĪŖ18£¬Š“³öøĆŗĖĖŲµÄ±ķŹ¾·ūŗÅ_____________”£
£Ø4£©AÓėC”¢CÓėFŌŖĖŲ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŅĄ“ĪĪŖ£ŗ_____________”¢_____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖæÉÄę·“Ó¦2SO2+ O22SO3£¬µ±Éś³É2 mol SO3Ź±·Å³öČČĮæĪŖQ£¬ĻÖ½«1 mol SO2ŗĶ0.5 mol O2ŌŚĻąĶ¬Ģõ¼žĻĀ·“Ӧɜ³ÉSO3·Å³öµÄČČĮæĪŖQ1£¬Ōņ
A.Q1=![]() QB.Q1<
QB.Q1<![]() QC.2Q1>QD.ĪŽ·ØÅŠ¶Ļ
QC.2Q1>QD.ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com