
| A. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| B. | 聚乙炔用I2或Na等做掺杂处理后可形成一种导电塑料,该导电塑料是一种纯净物 | |
| C. | 用蘸有浓氨水的棉棒检验输送氯气的管道是否漏气 | |
| D. | 用合成聚碳酸酯可降解塑料,实现“碳”的循环利用 |
分析 A.雾分散剂是空气,分散质为灰尘颗粒,活性炭具有吸附作用;
B.混合物不具有固定熔沸点;
C.3Cl2+8NH3═N2+6NH4Cl,该反应中产生白烟;
D.利用CO2合成聚碳酸酯类可降解塑料,减少二氧化碳的排放;
解答 解:A.雾分散剂是空气,分散质为灰尘,是分散系,活性炭具有吸附作用,带活性炭口罩防雾霾是利用了活性炭具有吸附性,能吸附可吸入性颗粒物等,故A正确;
B.聚乙炔用I2或Na等做掺杂处理后可形成一种导电塑料,属于混合物,无固定的熔沸点,故B错误;
C.3Cl2+8NH3═N2+6NH4Cl,利用该反应中产生白烟现象来检验氯气管道是否漏气,故C正确;
D.利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用应用,减少二氧化碳的排放,符合题意,故D正确;
故选:B.
点评 本题考查了化学与生活、社会密切相关知识,涉及分散系概念、氯气与氨气的性质、聚合物的组成及性质,熟悉相关概念及物质的性质是解题关键,注意对相关知识的积累.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S$→_{点燃}^{O_{2}}$SO3$\stackrel{H_{2}O}{→}$ H2SO4 | |
| B. | Fe $→_{点燃}^{Cl_{2}}$ FeCl2$\stackrel{NaOH溶液}{→}$ Fe(OH)2 | |
| C. | AlCl3(溶液)$\stackrel{蒸发}{→}$ AlCl3$\stackrel{电解}{→}$ Al | |
| D. | NaCl(饱和溶液)$\stackrel{依次通入NH_{3}、CO_{2}}{→}$ NaHCO3$\stackrel{△}{→}$Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 若a>b,一定存在c(A-)=c(K+) | B. | 若a=2b,一定存在c(A-)>c(K+) | ||
| C. | 若2a=b,一定存在c(OH-)>c(A-) | D. | 若a=b,一定存在c(OH-)=c(H+)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
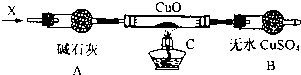
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
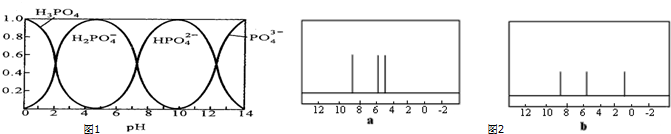
 ;分子N中含有2个手性碳原子.
;分子N中含有2个手性碳原子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
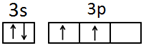 .
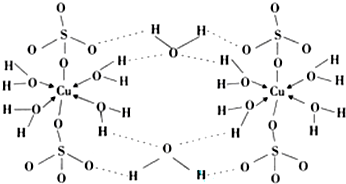
.
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 3s2和3s23p5 | B. | 2s22p2和2s22p4 | C. | 1s1和3s23p4 | D. | 3s23p4和2s22p4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com