
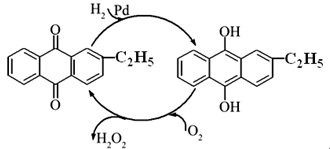
| 实验编号 | T/℃ | H2O2初始浓度/ mol·L-1 | FeCl3初始浓度/ mol·L-1 |
| Ⅰ | 20 | 1.0 | |
| Ⅱ | 50 | 1.0 | 0 |
| Ⅲ | 50 | | 0.1 |
| | 第一次 | 第二次 | 第三次 | 第四次 |
| 体积(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源:不详 题型:实验题
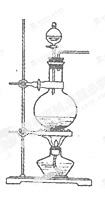
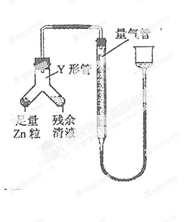
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
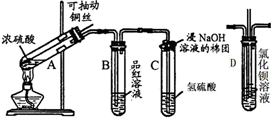
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
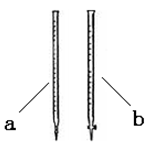
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.将配好的稀硫酸倒入试剂瓶中,贴好标签; |
| B.盖好容量瓶塞,反复颠倒,摇匀; |
| C.用量筒量取ml的18.0mol·L-1的浓硫酸; |
| D.将浓硫酸沿烧杯内壁慢慢注入盛有少量水的烧杯中; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 NaCl杂质,为测
NaCl杂质,为测 定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。
定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。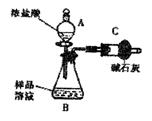
 可重复使用,夹持仪器略)
可重复使用,夹持仪器略)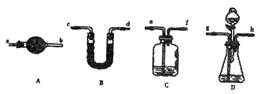
选用的 仪器 仪器 | | | | | |
| 添加的药品及必要的操作 | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.配制NaOH标准液时,所用的NaOH固体中含有少量的KOH杂质 |
| B.滴定前对碱式滴定管仰视读数,滴定后又俯视 |
| C.滴定前,碱式滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D.碱式滴定管用蒸馏水洗净后,直接装入标准NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
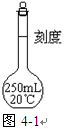
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定 次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com