
 2NO2��ƽ�⡣��ͼ�Ǹ�һ��ʱ��ⶨ����N2O4��Ũ�ȣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩
2NO2��ƽ�⡣��ͼ�Ǹ�һ��ʱ��ⶨ����N2O4��Ũ�ȣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩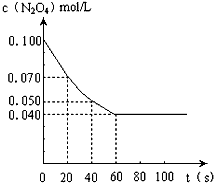
��1��������20��40��ʱ���ڣ�NO2��ƽ����������Ϊ____________mol��L-1��s-1��
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=____________��
��3���±��Dz�ͬ�¶��²ⶨ�õ��ĸ÷�Ӧ�Ļ�ѧƽ�ⳣ����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���¶�Ϊ373Kʱ����0.100mol��ɫ��N2O4�������1L��յ��ܱ������У����̳��ֺ���ɫ��ֱ������N2O4?2NO2��ƽ�⣮��ͼ�Ǹ�һ��ʱ��ⶨ����N2O4��Ũ�ȣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩
���¶�Ϊ373Kʱ����0.100mol��ɫ��N2O4�������1L��յ��ܱ������У����̳��ֺ���ɫ��ֱ������N2O4?2NO2��ƽ�⣮��ͼ�Ǹ�һ��ʱ��ⶨ����N2O4��Ũ�ȣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩| c2(NO2) |
| c(N2O4) |
| c2(NO2) |
| c(N2O4) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���¶�Ϊ373Kʱ����0.100mol��ɫ��N2O4�������1L��յ��ܱ������У����̳��ֺ���ɫ��ֱ������N2O4
���¶�Ϊ373Kʱ����0.100mol��ɫ��N2O4�������1L��յ��ܱ������У����̳��ֺ���ɫ��ֱ������N2O4  2NO2��ƽ�⣮��ͼ�Ǹ�һ��ʱ��ⶨ����N2O4��Ũ�ȣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩
2NO2��ƽ�⣮��ͼ�Ǹ�һ��ʱ��ⶨ����N2O4��Ũ�ȣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩| C2(NO2) |
| C(N2O4) |
| C2(NO2) |
| C(N2O4) |
| T/K | 323 | 373 |
| Kֵ | 0.022 | 0.36 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(14��) ���¶�Ϊ373Kʱ����0.400 mol��ɫ��N2O4����ͨ��4 L���
���ܱ������У����̳��ֺ���ɫ��ֱ������N2O4 2NO2 ��ƽ
�⡣��ͼ�Ǹ�һ��ʱ��ⶨ����N2O4��Ũ�ȣ�������ΪN2O4��Ũ�ȣ�
������Ϊʱ�䣩��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK = �����¶���,Kֵ= ��
��2��������0��20��ʱ���ڣ�NO2��ƽ����������Ϊ mol•L��1•s��1��
��3���±��Dz�ͬ�¶��²ⶨ�õ��ĸ÷�Ӧ�Ļ�ѧƽ�ⳣ����
| T/ K | 323 | 373 |
| Kֵ | 0.022 | �� |
�ݴ˿��Ʋ�÷�Ӧ������NO2���� ��Ӧ��ѡ����ȡ����ȡ�����
��4���������������䣬��Ӧ��373Kʱ�ﵽƽ���N2O4��NO2��Ũ�ȶ�������0.4mol/L��ƽ�⽫�� ����������桱����Ӧ�����ƶ���
(5) ��Ӧ��373Kʱ�ﵽƽ��ʱ��N2O4��ת����=_________________,������Ӧ�������ݻ���СΪԭ����һ�룬��N2O4��ת���ʽ�_________(ѡ���������С�����䡱)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10�֣����¶�Ϊ373Kʱ����0.25moi NO2����ͨ�����Ϊ500ml������ܱ������У�������Ӧ��2NO2(g)![]() N2O4(g).��Ӧ���е�2sʱ��N2O4����Ϊ0.05mol�����е�60sʱ���ﵽ�������·�Ӧ������ȣ���ʱ�����л�������ƽ����Է�������Ϊ47.5����
N2O4(g).��Ӧ���е�2sʱ��N2O4����Ϊ0.05mol�����е�60sʱ���ﵽ�������·�Ӧ������ȣ���ʱ�����л�������ƽ����Է�������Ϊ47.5����
��1����ʼʱ2s����c (NO2)�ı仯��ʾ�ķ�Ӧ�����Ƕ���?
��2���ﵽ�����ʱ��ϵ�ڵ�ѹǿ�ǿ�ʼ�Ķ��ٱ�?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010������ʡ�߶����ڲ��νο��Ի�ѧ���� ���ͣ�������
��10�֣����¶�Ϊ373Kʱ����0.25moi NO2����ͨ�����Ϊ500ml������ܱ������У�������Ӧ��2NO2(g)
 N2O4(g)
.��Ӧ���е�2sʱ��N2O4����Ϊ0.05mol�����е�60sʱ���ﵽ�������·�Ӧ������ȣ���ʱ�����л�������ƽ����Է�������Ϊ47.5����
N2O4(g)
.��Ӧ���е�2sʱ��N2O4����Ϊ0.05mol�����е�60sʱ���ﵽ�������·�Ӧ������ȣ���ʱ�����л�������ƽ����Է�������Ϊ47.5����
��1����ʼʱ2s����c (NO2)�ı仯��ʾ�ķ�Ӧ�����Ƕ���?
��2���ﵽ�����ʱ��ϵ�ڵ�ѹǿ�ǿ�ʼ�Ķ��ٱ�?
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com