
【题目】读图、读表是高中学生需要具备的重要能力。下列关于各图象的解读正确的是( )

A. 由甲推知氢气的燃烧热为219.8kJmol-1
B. 由乙推知离子反应Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)可以发生
C. 由丙可知:将A、B饱和溶液分别由T1℃升温T2℃时,溶质的质量分数:B>A
D. 由丁可知:同温度、同浓度NaA溶液与NaB溶液相比,其pH:NaA>NaB
【答案】B
【解析】A.1mol氢气完全燃烧生成液态水放出的热量为燃烧热,甲图中生成的产物为气态水,所以不能计算燃烧热,故A错误;B.原电池反应一定是自发的氧化还原反应,Co2+与Cd能发生原电池反应,则离子反应Co2+(aq)+Cd(s)═Co(s)+Cd2+(aq)可以发生,故B正确;C.T1℃时,A和B的溶解度相同,饱和溶液中溶质的质量分数相同,当升温到T2℃时,两者的溶解度均变大,无晶体析出,故溶液中的溶质的质量分数均不变,仍相等,故C错误;D.从图像可以看出,加水稀释时,HA的pH变化大,故HA的酸性强于HB,而酸越弱,其对应的盐越水解,故同温度、同浓度的NaA溶液与NaB溶液相比,NaB的水解程度大,pH更大,其pH前者小于后者,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】某同学研究浓度对化学平衡的影响,下列说法正确的是
已知: | |
步骤:
| 现象: 待试管b中颜色不变后与试管a比较,溶液颜色变浅。 滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深。 |
A. 该反应是一个氧化还原反应
B. 待试管b中溶液颜色不变的目的是使![]() 完全反应
完全反应
C. 该实验不能证明减小生成物浓度,平衡正向移动
D. 试管c中的现象说明影响平衡的主要因素是温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将a L HCl完全溶于水得到V mL盐酸,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是
①c=![]() ×100% ②c=
×100% ②c=![]() ③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w ④将50 g上述溶液加入一定量的水稀释成0.5c mol·L-1,则加入水的体积应大于50 mL
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w ④将50 g上述溶液加入一定量的水稀释成0.5c mol·L-1,则加入水的体积应大于50 mL
A. ①④ B. ②③
C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲是CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液;图乙是用H2还原CO2制备甲醇的工作原理示意图,硫酸为电解质溶液。下列说法不正确的是
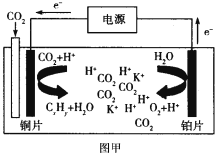

A.甲中铜片作阴极,K+向铜片电极移动
B.乙中正极发生的电极反应为CO2+6e-+6H+![]() CH3OH+H2O
CH3OH+H2O
C.乙中H2SO4的作用是增强溶液的导电性
D.甲中若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为___________。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
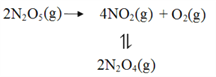
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O4(g)完全分解):
t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
p/kPa | 35.8 | 40.3 | 42.5. | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=4.4 kJ·mol1
2NO2(g)=N2O4(g) ΔH 2=55.3 kJ·mol1
则反应N2O5(g)=2NO2(g)+ ![]() O2(g)的ΔH=_______ kJ·mol1。
O2(g)的ΔH=_______ kJ·mol1。
②研究表明,N2O5(g)分解的反应速率![]() 。t=62 min时,测得体系中
。t=62 min时,测得体系中![]() pO2=2.9 kPa,则此时的
pO2=2.9 kPa,则此时的![]() =________kPa,v=_______kPa·min1。
=________kPa,v=_______kPa·min1。
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____63.1 kPa(填“大于”“等于”或“小于”),原因是________。
④25℃时N2O4(g)![]() 2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5![]() NO2+NO3 快速平衡
NO2+NO3 快速平衡
第二步 NO2+NO3→NO+NO2+O2 慢反应
第三步 NO+NO3→2NO2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______(填标号)。
A.v(第一步的逆反应)>v(第二步反应)
B.反应的中间产物只有NO3
C.第二步中NO2与NO3的碰撞仅部分有效
D.第三步反应活化能较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取软锰矿石(主要成分为MnO2)116g 跟足量浓盐酸发生如下反应(杂质不参与反应)MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,制得22.4L Cl2(标准状况)。下列有关说法中不正确的是
MnCl2+Cl2↑+2H2O,制得22.4L Cl2(标准状况)。下列有关说法中不正确的是
A.这种软锰矿石中MnO2的质量分数为75%
B.被氧化的HCl的物质的量为4mol
C.参加反应的HCl的质量为146g
D.被还原的MnO2的物质的量为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. π键是由两个p轨道“头碰头”重叠形成的
B. σ键就是单键,π键就是双键
C. 乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键
D. H2分子中含σ键,而Cl2分子中含π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼、镁及其化合物在工农业生产中应用广泛。
已知:硼镁矿主要成分为Mg2B2O5H2O,硼砂的化学式为Na2B4O710H2O,利用硼镁矿制取金属镁及粗硼的工艺流程为:

回答下列有关问题:
(1)硼砂中B的化合价为______ ,溶于热水后,常用H2SO4调pH 2~3制取H3BO3,反应的离子方程式为 _____________________________________,X为H3BO3晶体加热脱水的产物,其与Mg制取粗硼的化学方程式为 __________________。
(2)MgCl27H2O需要在HCl氛围中加热,其目的是 _______________________________。
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+=Mg2++2H2O,则正极反应式为________________;若起始电解质溶液pH=1,则pH=2时溶液中Mg2+离子浓度为______ 。已知Ksp[Mg(OH)2]=5.6×10-12,当溶液pH=6时,_______(填“有”或“没有”)Mg(OH)2沉淀析出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质能相互反应得到Al(OH)3的是
A. Al跟NaOH溶液共热
B. Al(NO3)3跟过量的NaOH溶液
C. Al2O3和水共热
D. Al2(SO4)3和过量的氨水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com