
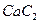 与水反应生成乙炔。
与水反应生成乙炔。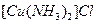 溶液生成
溶液生成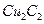 红棕色沉淀。
红棕色沉淀。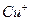 基态核外电子排布式为 。
基态核外电子排布式为 。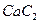 中
中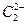 与
与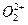 互为等电子体,
互为等电子体,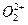 的电子式可表示为 ;1mol
的电子式可表示为 ;1mol 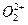 中含有的
中含有的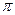 键数目为 。
键数目为 。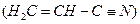 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
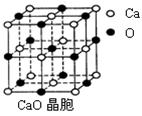
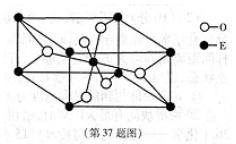
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。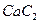 晶体的晶胞结构与
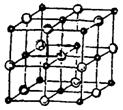
晶体的晶胞结构与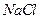 晶体的相似(如下图所示),但
晶体的相似(如下图所示),但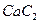 晶体中含有的哑铃形
晶体中含有的哑铃形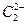 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。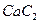 晶体中1个
晶体中1个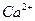 周围距离最近的
周围距离最近的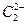 数目为
数目为  。
。
 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属晶体是由金属阳离子和自由电子构成的,它们都占据在晶胞的一定位置上 |
| B.六方最密堆积和面心立方最密堆积的空间利用率相同 |
| C.金属晶体在固态或熔融态均能导电 |
| D.温度升高,金属的导电性将减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
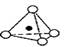 ,其中O表示氧原子,中心黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子。下图为某无限长单链的多聚硅酸根离子:
,其中O表示氧原子,中心黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子。下图为某无限长单链的多聚硅酸根离子: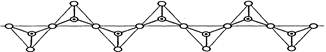
| A.1︰2 | B.1︰3 | C.1︰4 | D.2︰5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.晶体中分子间作用力越大,分子越稳定 |
| B.分子中共价键越强,该物质熔点越高 |
| C.铁熔化时金属键被破坏 |
| D.氯化钠溶于水时离子键未被破坏 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.物质的沸点:HF<HCI<BBr <HI |
| B.物质的熔点:汞<冰<食盐<石英 |
C.结合H+的能力:SO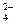 < CH3COO-<CO < CH3COO-<CO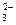 |
| D.分散系中分散质粒子的直径:FeCl3;溶液<Fe(OH3胶体<+Fe(OH3悬浊液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碘和氯化钾 | B.金刚石和重晶石 |
| C.二氧化硅和干冰 | D.软脂酸甘油酯和冰醋酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com