
如图所示,若电解5min时铜电极质量增加2.16g,试回答:
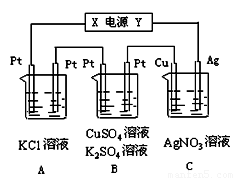
⑴ 电源电极X名称为____________。
⑵ pH变化:A池________,B池_______,C池________。
⑶ 通过5min时,B中共收集224mL气体(标 况),溶液体积为200mL,则通电前硫酸铜溶
液的物质的量浓度为______________。
⑷ 若A中KCl溶液的体积也是200mL,电解后溶液的pH = ______。
(10分)⑴ 负极(2分) ⑵ 增大,减小,不变 (各2分)
⑶ 0.025mol/L (1分) ⑷ 13(1分)
【解析】
试题分析:⑴电解5min时铜电极质量增加2.16g,说明了在C中,铜极析出了银,故铜极为阴极,而Ag极为阳极,所以电源的X为负极,而Y为正极;⑵ A池为电解氯化钾溶液,其原理与电解食盐水一样,故A池的pH增大,而B中左边则析出铜,而右边则析出氧气,产生了大量的氢离子,所以B池的pH减小,而C池中银溶解而在铜极上析出,故C池的pH不变;⑶电解5min时铜电极质量增加2.16g,则该电路通过的电子为
2.16/108=0.02mol,B收集的气体为氧气和氢气的混合物,氧气为0.02/4=0.005mol,氢气的物质的量为0.224/22.4-0.005=0.005,所以析出铜的物质的量n=(0.02-0.005×2)/2=0.005mol,故通电前硫酸铜溶
液的物质的量浓度为0.005/0.2= 0.025mol/L;⑷ A中发生的反应为:2KCl+2H2O=H2↑+2KOH,该反应转移的电子数为2,但有0.02mol电子通过是,生成了0.02molKOH,所以氢氧根的浓度为0.02/0.2=0.1,所以电解后该溶液的pH为13。
考点:电解池
点评:本题考查了电解池的判断,以及相关的计算,该考点是高考考查的重点和难点,本题的难度设计比较好,一步一步递增,该题难度中等。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 如图所示,若电解5min时,测得铜电极的质量增加2.16g.
如图所示,若电解5min时,测得铜电极的质量增加2.16g.
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
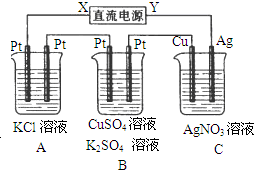 如图所示,若电解5min时,测得铜电极的质量增加2.16g,试回答:
如图所示,若电解5min时,测得铜电极的质量增加2.16g,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
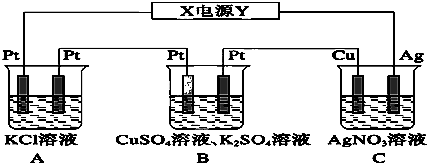
查看答案和解析>>
科目:高中化学 来源: 题型:
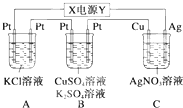 如图所示,若电解5min时,测得铜电极的质量增加2.16g.试回答:
如图所示,若电解5min时,测得铜电极的质量增加2.16g.试回答:查看答案和解析>>
科目:高中化学 来源:2012-2013学年新疆兵团农二师华山中学高二上学期期末考试化学试卷(带解析) 题型:填空题
如图所示,若电解5min时铜电极质量增加2.16g,试回答:
⑴ 电源电极X名称为____________。
⑵ pH变化:A池________,B池_______,C池________。
⑶ 通过5min时,B中共收集224mL气体(标 况),溶液体积为200mL,则通电前硫酸铜溶
液的物质的量浓度为______________。
⑷ 若A中KCl溶液的体积也是200mL,电解后溶液的pH = ______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com