
A、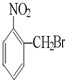 |
B、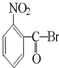 |
C、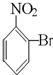 |
D、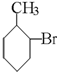 |
 水解生成
水解生成 ,为醇类物质,不具有酸性,不能与碳酸氢钠反应,故A错误;
,为醇类物质,不具有酸性,不能与碳酸氢钠反应,故A错误; 水解生成
水解生成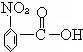 ,酸性比碳酸强,可与碳酸氢钠反应,故B正确;
,酸性比碳酸强,可与碳酸氢钠反应,故B正确; 水解生成
水解生成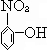 ,酚羟基比碳酸弱,不能与碳酸氢钠反应,故C错误;
,酚羟基比碳酸弱,不能与碳酸氢钠反应,故C错误; 水解生成
水解生成 ,为醇类物质,不具有酸性,不能与碳酸氢钠反应,故D错误.
,为醇类物质,不具有酸性,不能与碳酸氢钠反应,故D错误.

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作和现象 | 结论 | |
| A | 向用盐酸酸化的FeCl2溶液的试管中加入少量NaNO2溶液,在管口观察到红棕色气体 | 主要原因是: H++NO2-=HNO2, 2HNO2=NO↑+NO2↑+H2O |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成. | 淀粉没有水解成葡萄糖 |
| C | 向阿司匹林(乙酰水杨酸)中加足量饱和NaHCO3溶液,有大量气泡产生. | 阿司匹林彻底水解 |
| D | 向1mL1.0mol?L-1AlCl3溶液中滴加2mL10% NH4F溶液,再滴加1mL 3.0mol?L-1NH3?H2O溶液,无沉淀生成. | Al3+更易与F-结合成AlF63- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
| A、溶液中由水电离出的c(OH-)=1×10-10mol/L |
| B、溶液中c(OH-)+c(NH3?H2O)=0.1mol/L |
| C、与0.1mol/L 的盐酸等体积混合后所得溶液中:c(Cl-)=c(NH4+)+c(NH3?H2O)=0.1mol/L |
| D、原溶液中加入少量的氯化铵晶体或加水稀释,溶液中的c(H+)均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将②、③溶液混合后,pH=7,消耗溶液的体积:②>③ |
| B、①④等体积混合后,溶液显碱性 |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量①最大 |
| D、向溶液中加入100mL水后,溶液的pH:③>④>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 |
| B、100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速度减小 |
| C、SO2的催化氧化是一个放热的反应,所以升高温度,V逆加快,V正减慢 |
| D、对于CaCO3+2HCl═CaCl2+H2O+CO2↑不能用CaCO3的浓度变化来表示反应速率,但可用水的浓度变化来表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MnO2+4HCl=MnCl2+2H2O+Cl2↑ | ||||
| B、2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | ||||
| C、5Cl2+I2+6H2O=10HCl+2HIO3 | ||||
D、2NaCl+2H2O
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com