
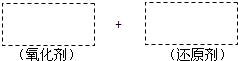
 ;
; ;
; ;
; ;
;

科目:高中化学 来源: 题型:
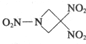
| A、分子中N、O间形成的共价键是非极性键 |
| B、该物质既有氧化性又有还原性 |
| C、C、N、O的第一电离能从大到小的顺序为O>N>C |
| D、C、N、0的气态氢化物的沸点依次降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
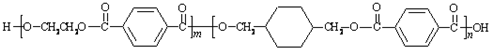
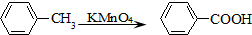
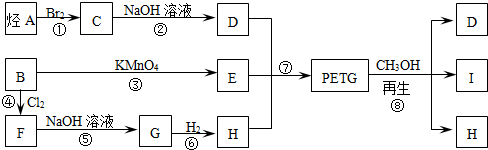
查看答案和解析>>
科目:高中化学 来源: 题型:

 )和多巴胺的结构相似,它的核磁共振氢谱中可以发现有
)和多巴胺的结构相似,它的核磁共振氢谱中可以发现有查看答案和解析>>
科目:高中化学 来源: 题型:
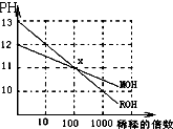
| A、在x点,ROH未完全电离 |
| B、在x点,c(M+)>c(R+) |
| C、稀释前,c(ROH)=10c(MOH) |
| D、pH=2的盐酸与pH=12的MOH等体积混合后,溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
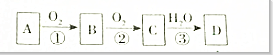 A、B、C、D四种物质的转化关系如图所示(反应条件及其产物乙略去),请回答下列问题:
A、B、C、D四种物质的转化关系如图所示(反应条件及其产物乙略去),请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
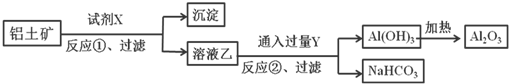
| A、反应①中试剂X是氢氧化钠溶液 |
| B、反应①、过滤后所得沉淀为氢氧化铁 |
| C、图中所示转化反应中包含一个氧化还原反应 |
| D、将试剂X和Y进行对换,最终可以达到相同的效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液 |
| B、乙醇(水):加入新制生石灰,蒸馏 |
| C、溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 |
| D、乙酸(乙醇):加入金属钠,蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com