
利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均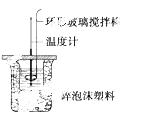 匀,测得混合液最高温度
匀,测得混合液最高温度 。回答下列问题:
。回答下列问题:
(1)为什么所用NaOH溶液要稍过量?__________________
________________________________________________________。
(2)倒入NaOH溶液的正确操作是__________(填序号)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是________(填序号)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为________________。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为 了计算中和热,某学生实验记录数据如下:
了计算中和热,某学生实验记录数据如下:
| 实验序号 |
| 终止温度t2/ ℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__________(结果保留一位小数)。
(6)________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是____________________________________________________________。
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
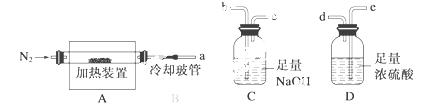
氯离子插层镁铝水滑石[Mg2Al(OH)6Cl·xH2O]是一种新型离子交 换材料,其在高温下完全分解为MgO、Al2O3、HCl和水蒸气。现用下图装置进行实验确定其化学式(固定装置略去)。
换材料,其在高温下完全分解为MgO、Al2O3、HCl和水蒸气。现用下图装置进行实验确定其化学式(固定装置略去)。
(1)Mg2Al(OH)6Cl·xH2O热分解的化学方程式为________________________________。
(2)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为__________(按气流方向,用接口字母表示),其中C的作用是____________。装置连接后,首先要进行的操作的名称是____________。
(3)加热前先通N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2的作用是________、________等。
(4)完全分解后测得C增重3.65 g 、D增重9.90 g ,则x=__________。若取消冷却玻管B后进行实验,测定的x值将________(填“偏高”或“偏低”)。
(5)上述水滑石在空气中放置时易发生反应生成[Mg2Al(OH)6Cl1-2y·(CO3)y·zH2O],该生成物能发生类似的热分解反应。现以此物质为样品,用(2)中连接的装置和试剂进行实验测定 z,除测定D的增重外,至少还需测定__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛。
(1)C60分子中每个原子接2个单键和一个双键,它与F2发生加成反应,其加成产物的分子式为 ;C60的晶体结构类似于干冰,则每个C60晶胞的质量为 (用含NA的式子表示)。
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是 。
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有( )
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C—C<石墨中C—C;
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力;
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
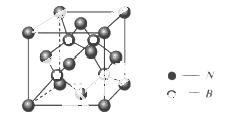
(4)立方BN结构与金刚石相似,晶胞结构如下图,在BN晶体中,B原子周围最近的N原子所构成的立体图形为 ,B原子与N原子之间共价键与配位键的数目比为 ,一个晶胞中N原子数目为 。
(5)碳与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为 ,金属铜采用面心立方最密堆积,则Cu的晶体中Cu原子的配位数为 。已知Cu单质的晶体密度为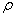 g•cm-3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为 。
g•cm-3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的原子半径为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.物 质发生化学反应都伴随着能量变化
质发生化学反应都伴随着能量变化
B.伴有能量变化的物质变化都是化学变化
C.在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同
D.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
在强光持续照射下,向含28.6 g  CaClO2的漂白粉悬浊液中通入1.12 L CO2标准状况下,可产生标准状况下的氧气体积是
CaClO2的漂白粉悬浊液中通入1.12 L CO2标准状况下,可产生标准状况下的氧气体积是
A.1.12 L B.2.24 L C.3.36 L D.4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
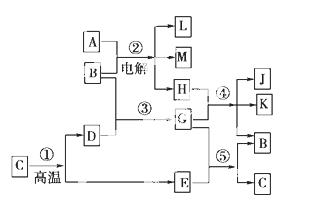
(1)单质L是______________。
(2)化合物B是______________。
(3)图中除反应①以外,还有两个用于工业生产的反应,是______________和__________(填代号)。它们的化学反应方程式分别是________和________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时,所克服的粒子间作用力与氮化硅熔化时所克服的作用力相同的是( )
A.NaNO3和金刚石 B.晶体硅和石英
C.Cu和MgCl2 D.蔗糖和碘
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室要用CuSO4·5H2O晶体配制500 mL 0.1 mol·L-1 CuSO4溶液,回答下列问题:
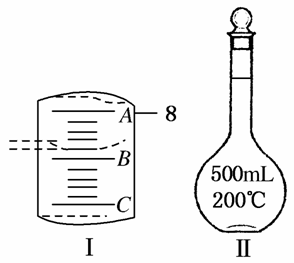
(1)应该用托盘天平称取CuSO4·5H2O________g。
(2)如图Ⅰ表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为8,量筒中液体的体积是________mL。
(3)若实验中如图Ⅱ所示的仪器有下列情况,对配制溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.定容前容量瓶底部有水珠__________________________;
B.定容时加水超过刻度线____________________________;
C.最终定容时俯视观察液面__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com