
| A�� | �٢ڢ� | B�� | �ܢ� | C�� | �ڢܢ� | D�� | �ڢ� |
���� ��������һ�����ʵ���Ũ����Һһ�㲽�裺���㡢�������ܽ⡢��ȴ��ϴ�ӡ����ݡ�ҡ�ȵȲ������������ƽ������ƿʹ�÷�����ע��������
��� �⣺����һ�����ʵ���Ũ����Һһ�㲽�裺���㡢�������ܽ⡢��ȴ��ϴ�ӡ����ݡ�ҡ�ȵȣ�
����������Ϊ��ʴƷ��Ӧ����С�ձ��г������ʴ���
�����ձ��м���Լ300mL����ˮ���ò���������ʹ֮��ȫ�ܽ⣬����ȷ��
������ƿΪ��������������ʢ�Ź�����߹���Һ�壬�����ܽ��Ӧ����Һ��ȴ�����£��ٽ��ձ��е���Һ�ز�����ע��1000mL������ƿ�У��ʴ���
�ܽ��Ž�����ƿ���ȣ�Ȼ�������ˮ��Һ��ӽ��̶�1cm��2cm��������ȷ��
���ý�ͷ�ιܼ�����ˮ��ʹ��Һ��Һ��ǡ����������У�������ȷ������ȷ��
������ƿ������ҡ�ȣ����ã���ʱ��Һ����ڿ̶��ߣ������ٵμ�����ˮ���ʴ���
��ѡ��C��
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƣ���ȷ����ԭ�������������ǽ���ؼ���ע������ƿʹ�÷�����ע�������Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϡ��ˮ��ͨ�����CO2��NH3•H2O+CO2�TNH4++HCO3- | |
| B�� | ����ϡHNO3��Ӧ��Fe+2H+=�TFe2++H2�� | |
| C�� | ��ϡHNO3�ܽ�FeS���壺FeS+2H+�TFe2++H2S�� | |
| D�� | ���Ȼ�������Һ��ϡ�����ϣ�Fe2++4H++NO3-�TFe3++2H20+NO�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������̷� | B�� | Һ�������� | ||
| C�� | �ɱ�����þ60%������þ | D�� | ֲ���͡����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ��1���£�N2H4���ֳ���������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϣ���֪��100kPaʱ��32.0g N2H4����������ȫȼ�����ɵ������ų�����624kJ��25�棩��N2H4��ȫȼ�յ��Ȼ�ѧ����ʽ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��l����H=-642kJ/mol��
��1���£�N2H4���ֳ���������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϣ���֪��100kPaʱ��32.0g N2H4����������ȫȼ�����ɵ������ų�����624kJ��25�棩��N2H4��ȫȼ�յ��Ȼ�ѧ����ʽ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��l����H=-642kJ/mol���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ����β���dz��е���Ҫ������Ⱦ��о���������β����Ϊ������������Ҫ����
����β���dz��е���Ҫ������Ⱦ��о���������β����Ϊ������������Ҫ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
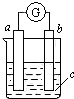
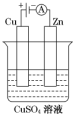
| A�� | a��п��b��ͭ��c��������Һ | B�� | a������b������c����������Һ | ||
| C�� | a������b������c����������Һ | D�� | a������b��̼��c���Ȼ�ͭ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٣��ڣ��ۣ��� | B�� | �ܣ��ۣ��ڣ��� | C�� | �ܣ��ۣ��٣��� | D�� | �٣��ܣ��ۣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �Ȼ�����ʵ�����е���Ҫ�Լ���ijͬѧ��m g�������⣨Fe2O3���ķ���м����ȡFeCl3•6H2O���壬ͬʱ�ⶨ����м����������������Ϊ�����������װ�ã��г�װ���ԣ��������Ѽ��飩��
�Ȼ�����ʵ�����е���Ҫ�Լ���ijͬѧ��m g�������⣨Fe2O3���ķ���м����ȡFeCl3•6H2O���壬ͬʱ�ⶨ����м����������������Ϊ�����������װ�ã��г�װ���ԣ��������Ѽ��飩���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com