
分析 (1)根据配制溶液的实验操作过程选择所需的仪器来判断;
(2)再根据溶液稀释前后物质的量不变计算所需浓硫酸的体积;
(3)分析操作对溶质物质的量、溶液体积的影响,根据c=$\frac{n}{V}$判断对溶液浓度的影响.
解答 解:(1)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.由提供的仪器可知不需要的仪器有:②烧瓶;④药匙;⑥托盘天平;还需要仪器有:100mL容量瓶、玻璃棒;
故答案为:②④⑥;100mL容量瓶、玻璃棒;
(2)根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,则有:
xmL×18.4mol/L=100mL×1mol/L,解得:x≈5.4,
故答案为:5.4;
(3)A.容量瓶中原来含有少量蒸馏水,对溶液的体积无影响,所配制溶液浓度不变,故A错误;
B.未经冷却,立即转移至容量瓶并洗涤烧杯,热的溶液体积偏大,冷却后溶液体积变小,导致配制的溶液体积偏小,所配制溶液浓度偏大,故B正确;
C.烧杯没有洗涤,导致配制的溶液中溶质的物质的量偏小,所配制溶液浓度偏小,故C错误;
D.向容量瓶中加水定容时眼睛一直仰视刻度线,液面超过刻度线,溶液的体积偏大,所配制溶液浓度偏小,故D错误;
故答案为:B.
点评 本题考查了溶液配制的方法,题目难度不大,明确配制方法为解答关键,注意掌握误差分析的方法与技巧,试题侧重基础知识的考查,培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:解答题
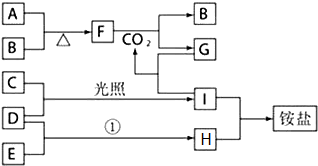 某兴趣小组的同学发现《高中化学(必修1)》中学习的单质及其化合物(或其溶液)存在如图的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;F为淡黄色粉末,化合物H和I通常状况下呈气体;反应①是化工生产中的一种重要固氮反应.
某兴趣小组的同学发现《高中化学(必修1)》中学习的单质及其化合物(或其溶液)存在如图的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;F为淡黄色粉末,化合物H和I通常状况下呈气体;反应①是化工生产中的一种重要固氮反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度 | B. | 增大压强 | C. | 充入一定量CO2 | D. | 再加入一些铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备乙酸乙酯的实验中,承接酯的小试管中盛放了一定量的氢氧化钠溶液 | |
| B. | 实验室制乙烯时应将无水乙醇缓慢加入到浓硫酸中 | |
| C. | 在酸性重铬酸钾溶液中加入少量乙醇,橙色溶液变红 | |
| D. | 为减缓反应速率,将饱和食盐水滴加到烧瓶中的电石上来制取乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用量筒量取浓盐酸配制0.01mol/L稀盐酸时,量筒用蒸馏水洗净后未经干燥直接量取浓盐酸 | |
| B. | 配制稀盐酸定容时,俯视容量瓶刻度线 | |
| C. | 滴定前尖嘴处无气泡,滴定终点时有气泡 | |
| D. | 滴定过程中用少量蒸馏水将锥形瓶内避粘附的盐酸冲下 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol氢气中含有氢原子的数目为0.3NA | |
| B. | 标准状况下,4.48L苯中含有苯分子的数目为0.2NA | |
| C. | 0.2mol•L-1CaCl2溶液中含有氯离子的数目为0.4NA | |
| D. | 1molNa2O2与足量水反应,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 可以与醋酸发生中和反应 | B. | 能发生催化氧化反应 | ||
| C. | 能使紫色石蕊试液变红色 | D. | 能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加水稀释、平衡①、②均向右移,溶液中c(HSO3-)、c(H)+均减小 | |
| B. | 加入少量NaOH溶液,$\frac{c(S{O}_{3}^{2-})}{c(HS{O}_{3}^{-})}$、$\frac{c(O{H}^{-})}{c({H}^{+})}$的值均增大 | |
| C. | 加入少量Na2SO3固体,则c(H+)+c(Na+)=c(${HSO}_{3}^{-}$)+c(OH-)+$\frac{1}{2}$c(${SO}_{3}^{2-}$) | |
| D. | 加入氨水至中性,则2c(Na+)=c(${SO}_{3}^{2-}$)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
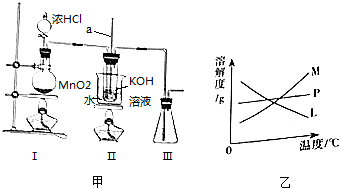
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com