
分析 (1)25℃时,Kw=10-14,某强酸溶液pH=a,则该酸溶液中氢离子浓度为10-a mol/L,强碱溶液pH=b,则碱溶液中氢氧根离子浓度=10 b-14 mol/L,混合后溶液的pH=7说明氢离子和氢氧根离子的物质的量相等,据此解答;
(2)酸碱混合后,pH=12,则碱过量,剩余的c(OH-)=0.01mol/L,以此来计算;
(3)根据纯水中c(OH-)=c(H+),溶液显示中性进行分析;根据该温度下纯水中氢离子浓度和氢氧根离子浓度,计算出水的离子积;若温度不变,根据稀硫酸溶液中氢离子浓度和水的离子积计算出溶液中氢氧根离子的浓度;若温度不变,依据氢氧化钠溶液中氢氧根离子浓度,结合离子积常数计算溶液中氢离子浓度.
解答 解:(1)25℃时,Kw=10-14,某强酸溶液pH=a,则该酸溶液中氢离子浓度为10-a mol/L,强碱溶液pH=b,则碱溶液中氢氧根离子浓度=10 b-14 mol/L,混合后溶液的pH=7说明氢离子和氢氧根离子的物质的量相等,设酸的体积为V(酸),碱的体积为V(碱),10-a mol/L×V(酸)L=10 b-14 mol/L×V(碱)L,则V(酸)=10 a+b-14 V(碱),而a+b=12,故V(碱)=102 V(酸);
故答案为:V(碱)=102 V(酸);
(2)设NaOH和HCl的物质的量浓度均为x,NaOH和HCl溶液以3:2体积比相混合,体积分别为3V、2V,
酸碱混合后,pH=12,则碱过量,剩余的c(OH-)=0.01mol/L,
则$\frac{3V×x-2V×x}{5V}$=0.01mol/L,
解得x=0.05mol/L;
故答案为:0.05 mol/L;
(3)纯水显示中性,c(OH-)=c(H+)=5.0×10-7mol/L;此温度下,水的离子积为:Kw=5.0×10-7×5.0×10-7=2.5×10-13,若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,硫酸溶液中氢离子浓度c(H+)=5.0×10-3mol/L,c(OH-)=$\frac{2.5×1{0}^{-13}}{5.0×1{0}^{-3}}$mol/L=5.0×10-11 mol/L,
在该温度时,往水中滴入NaOH溶液,溶液中的c(OH-)=5.0×10-2mol/L,则溶液中c(H+)=$\frac{2.5×1{0}^{-13}}{5.0×1{0}^{-6}}$mol/L=5×10-12mol/L,
故答案为:5.0×10-7mol/L;5.0×10-11mol/L;5×10-12mol/L.
点评 本题考查了离子积常数的有关计算,题目难度中等,根据溶液的酸碱性及水的离子积常数来分析解答,注意该温度下纯水中c(H+)=5×10-7mol/L,则水的离子积常数是2.50-13,为易错点.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
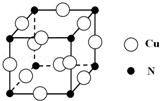 硼和氮元素在化学中有很重要的地位,回答下列问题:
硼和氮元素在化学中有很重要的地位,回答下列问题: .预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.
.预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.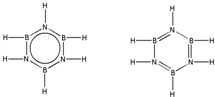 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O | B. | 2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ | ||
| C. | 2CO+O2═2CO2 | D. | 2Al+2NaOH+2H2O═2NaAlO2+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
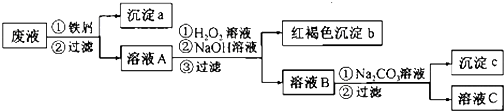
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 第Ⅱ步的离子方程式为Na++NH3+H2O+CO2→NaHCO3↓+NH4+ | |
| B. | 第Ⅲ步得到的晶体是Na2CO3•10H2O | |
| C. | A气体是CO2,B气体是NH3 | |
| D. | 第Ⅳ步操作的过程主要有溶解、蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
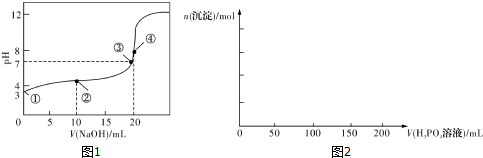
| n(SO32-):n(HSO3-) | 1:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准NaOH溶液读数记录(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 | 2.0×10-48 | 2.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com