
 (1)K4[Fe(CN)6]中Fe2+与CN-两种离子之间的作用力是配位键,基态Fe2+的电子排布式1s22s22p63s23p63d6 或[Ar]3d6 ,1molCN-中含有π键的数目为2NA.
(1)K4[Fe(CN)6]中Fe2+与CN-两种离子之间的作用力是配位键,基态Fe2+的电子排布式1s22s22p63s23p63d6 或[Ar]3d6 ,1molCN-中含有π键的数目为2NA.分析 (1)铁是26号元素,其原子核外有26个电子,铁原子失去2个电子变成Fe2+,根据构造原理书写Fe2+核外电子排布式,提供空轨道的原子和提供孤电子对的原子之间易形成配位键;CN-中含有三键,三键中含有两个π键;
(2)二甲醚(CH3OCH3)中氧原子形成2个共价键,还有两个孤电子对;CH3CH2OH含氢键,使其沸点升高;
(3)根据电负性的角度分析;
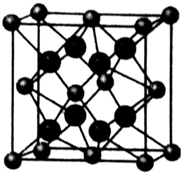
(4)O和Na形成的一种只含有离子键的离子化合物为Na2O,该晶胞结构中小球有8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,大球在内部,共有8个,所以小球为O2-,大球为Na+.
解答 解:(1)亚铁离子含有空轨道,N原子含有孤电子对,所以能形成配位键;铁是26号元素,其原子核外有26个电子,铁原子失去最外层2个电子变成Fe2+,根据构造原理知,其基态离子核外电子排布式为1s22s22p63s23p63d6 或[Ar]3d6 ,CN-中含有三键,三键中含有两个π键,则1molCN-中含有π键的数目为2NA;
故答案为:配位键;1s22s22p63s23p63d6 或[Ar]3d6 ;
(2)二甲醚(CH3OCH3)中氧原子形成2个共价键,还有两个孤电子对,所以氧原子的价层电子对数为4,其杂化方式为sp3;CH3CH2OH含氢键,使其沸点升高,CH3CH2OH的沸点高于CH3OCH3的沸点,
故答案为:sp3;低;
(3)N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与H+形成配离子;
故答案为:F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与H+形成配离子;
(4)O和Na形成的一种只含有离子键的离子化合物为Na2O,该晶胞结构中小球有8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,大球在内部,共有8个,所以小球为O2-,大球为Na+,以晶胞中上面心O2-离子为研究对象,距一个O2-周围最近的Na+离子有8个,位于晶胞中上层4个Na+及上面晶胞中的下层4个Na+,8个Na+离子形成立方体结构,
故答案为:立方体.
点评 本题考查知识点较多,为原子结构与性质的习题,涉及配位键、电子排布、共价键的类型、氢键对物质性质的影响、晶体结构及其计算,(4)为解答的难点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
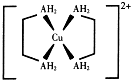 铜及其化合物在现代生活中应用广泛.
铜及其化合物在现代生活中应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期元素的离子半径从左到右逐渐减小 | |
| B. | 已知单质A能从溶液中置换出单质B,当A为非金属时,B也一定是非金属 | |
| C. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| D. | 同周期非金属元素氧化物对应水化物的酸性从左到右依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往鲜榨苹果汁中加入适量柠檬汁防止苹果汁变色 | |
| B. | 做馒头时加一些面碱(Na2CO3)避免馒头发酸 | |
| C. | 采用添加有“光触媒”的硅藻泥做装饰材料,净化室内空气,避免装修污染 | |
| D. | 用汽油洗掉衣物沾上的油渍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同分异构体因结构不同,化学性质一定差别很大 | |
| B. | 具有相同通式的有机物不一定互为同系物 | |
| C. | 两个相邻同系物的相对分子质量数值一定相差14 | |
| D. | 同分异构体不可能互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
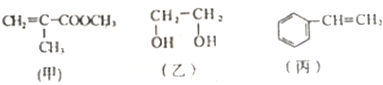
| A. | 甲物质可以在引发剂作用下生成有机高分子化合物 | |
| B. | 甲、乙、丙三种物质都可以发生加成反应 | |
| C. | 丙物质能够使酸性高锰酸钾溶液褪色 | |
| D. | 1mol乙物质可与2mol钠完全反应生成1mol氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
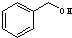 与
与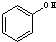 ⑥
⑥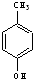 与
与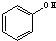
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
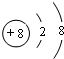 ,D元素在周期表中的位置是第三周期ⅥA族.
,D元素在周期表中的位置是第三周期ⅥA族.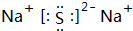 ,氢化物的稳定性是A>D(填“>”或“<”).
,氢化物的稳定性是A>D(填“>”或“<”).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com