
分析 (1)明矾在水中电离生成钾离子、铝离子、硫酸根离子;
(2)明矾电离出的硫酸根离子和钡离子反应生成硫酸钡沉淀;
(3)铝离子和一水合氨反应生成氢氧化铝沉淀,氢氧化铝不溶于弱碱;
(4)向明矾溶液中逐滴加入Ba(OH)2溶液,当Al3+恰好全部沉淀时,反应生成硫酸钡、氢氧化铝、硫酸钾.
解答 解:(1)明矾在水中电离生成钾离子、铝离子、硫酸根离子,则电离方程式为KAl(SO4)2=K++Al3++2SO42-,故答案为:KAl(SO4)2=K++Al3++2SO42-;
(2)明矾电离出的硫酸根离子和钡离子反应生成硫酸钡沉淀,离子反应方程式为Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓;
(3)铝离子和一水合氨反应生成氢氧化铝沉淀,氢氧化铝不溶于弱碱,离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(4)向明矾溶液中逐滴加入Ba(OH)2溶液,当Al3+恰好全部沉淀时,离子方程式为:2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓;
故答案为:2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓.
点评 本题考查离子方程式书写,为高频考点,明确物质性质及物质之间反应是解本题关键,注意(4)中产物成分与反应物的量有关,为易错点.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:填空题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
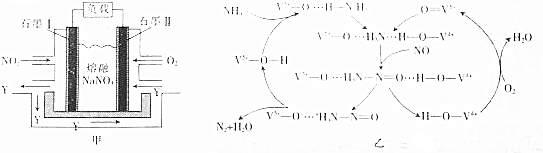
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
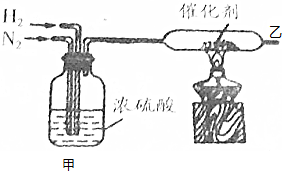
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验 序号 | t/min c/(mol•L-1) 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.50 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子式  可以表示甲基,但不能表示CH3+ 可以表示甲基,但不能表示CH3+ | |
| B. | 比例模型 既能表示甲烷分子,也能表示四氯化碳分子 既能表示甲烷分子,也能表示四氯化碳分子 | |
| C. | C2H4O2可以表示乙酸、甲酸甲酯等物质 | |
| D. | 离子结构示意图 可以表示32S2-,也可以表示34S2- 可以表示32S2-,也可以表示34S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com