
| A. | 硬水、软水(肥皂水) | B. | 稀盐酸、食盐水(酚酞试液) | ||
| C. | 涤纶、羊毛制品(点燃) | D. | 空气、氧气(带火星的木条) |
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 一个该微粒含3个中子 | B. | 它是氢的一种新的同位素 | ||
| C. | 其组成可用H3+表示 | D. | 它比一个普通氢分子多一个氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15.5 mol | B. | 18 mol | C. | 20.5 mol | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
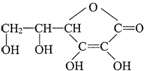 维生素C的结构简式是,它的分子式是C6H8O6;由于它能防治坏血病,又称为抗坏血酸.在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有酸性.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐.离子方程式为Fe+2H+═Fe2++H2↑.
维生素C的结构简式是,它的分子式是C6H8O6;由于它能防治坏血病,又称为抗坏血酸.在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有酸性.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐.离子方程式为Fe+2H+═Fe2++H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用玻璃棒搅拌漏斗中的液体以加快过滤速度 | |
| B. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| C. | 往煮沸的NaOH溶液中滴加饱和氯化铁溶液,可制取Fe(OH)3胶体 | |
| D. | 蒸馏时需从冷凝管上口进水,下口出水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br2>Fe3+>I2 | B. | I->Fe2+>Br- | C. | Br2>I2>Fe3+ | D. | Fe3+>I2>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、NH${\;}_{4}^{+}$、Cl-、H+ | B. | Fe2+、H+、CO${\;}_{3}^{2-}$、Cl- | ||
| C. | Fe3+、OH-、SO${\;}_{4}^{2-}$、Cl- | D. | Fe2+、Ca2+、NO${\;}_{3}^{-}$、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
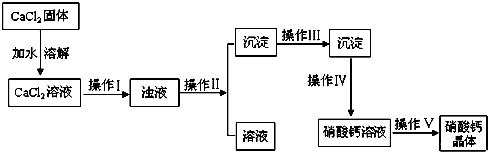
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com